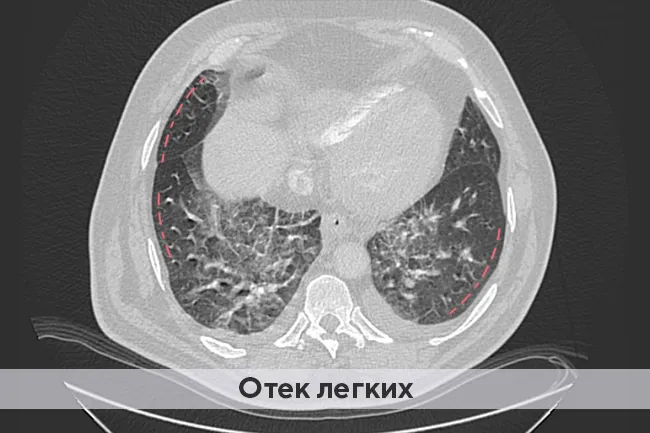
В медицинской терминологии метастазами называются вторичные очаги роста (отсевы) злокачественных опухолей. Жизнеспособные раковые клетки, оторвавшись от «материнского» новообразования и проникнув в просвет кровеносного или лимфатического сосуда, перемещаются и оседают в новом месте. Далее они начинают активно делиться, образуя метастатический очаг. Наиболее обширным по площади кровоснабжения внутренним органом считаются легкие, являющиеся одним из самых частых мест метастазирования опухолей. Кроме того, различные виды опухолей имеют тропность (тягу) к развитию метастазов в определенных органах, чаще такими органами служат, помимо легких, головной мозг, печень, кости.
Метастазирующие опухоли
Современная онкология располагает информацией о множестве первичных злокачественных новообразований, способных распространяться, образуя метастазы в легких и других органах. Данный список включает в себя:
- рак почки (16 %);
- рак молочной железы (8,2 %);
- рак толстой (прямая и ободочная) кишки (14,3 %);
- рак легкого (7,4 %);
- саркомы костей (24,1 %).
В ряде случаев первичная опухоль, спровоцировавшая отсев злокачественных клеток, остается неизвестной. Зачастую процесс метастазирования долгое время не дает о себе знать и обнаруживается только при диагностическом обследовании или на самой последней стадии заболевания.
Рак лёгкого и туберкулёз
Если пневмония исключена, обычно необходимо выполнить дифференциальную диагностику между раком лёгких и туберкулёзом. Схожесть симптоматики характерна для инфильтративного туберкулёза и периферического рака.
При туберкулёзе нередко можно выявить прямой контакт пациента с подтверждённым носителем микобактерий. Температура тела бывает повышенной в вечерние и ночные часы, вплоть до субфебрильной и фебрильной (в отличие от рака, при котором чаще всего температура не поднимается выше субфебрилитета). При онкологическом процессе чаще отмечается локализованный сухой кашель.
Течение туберкулёза обычно полисимптомно, но признаки выражены слабо, а при онкологическом процессе, как правило, можно явно выявить 1-2 основных симптома. При анализе мокроты патогномоничным признаком будет обнаружение возбудителей туберкулёза, а при раке — атипичных клеток (в большинстве случаев). Также специфический результат дадут подкожные туберкулиновые пробы, которые при инфицировании микобактериями дают положительный результат, а при злокачественных опухолях лёгкого — отрицательный.
Рентгенологически при туберкулёзной инфильтрации можно увидеть полисегментарные затемнения округлой или облаковидной формы, участки бронхогенного обсеменения в удалённых областях лёгкого или в другом лёгком. При ателектазе (который часто встречается при центральной форме рака) выявляется культя бронха, на фоне затемнения не видно светлых полосок бронхиального дерева (в отличие от туберкулёза).
Если сравнивать кавернозную форму туберкулёза с полостными образованиями при раке, то поначалу рентгенологически их отличить тяжело — в обоих случаях каверна имеет толстые неровные стенки с перифокальным воспалением и инфильтрацией, с наличием внутри жидкости. После отторжения некротических масс, стенки туберкулёзной каверны становятся более тонкими и ровными, само затемнение — округлое (ближе к правильной форме), а инфильтрация вокруг образования уменьшается.
Сложности могут возникнуть при дифференциальной диагностике узловой формы периферического рака и туберкуломы. Последняя имеет более чёткие округлые контуры, а рак имеет специфическую лучистость. Для туберкуломы характерны участки обызвествления и кальцификаты.
В любом случае, для дифференциального диагноза рака лёгких и туберкулёза чаще всего решающее значение имеют результаты биопсии.
Симптомы метастатического поражения легких
Одним из самых характерных симптомов метастазов в легких является кашель. Сначала он может протекать под маской затянувшегося бронхита, затем переходит в постоянный, сухой, надрывный и мучительный. В мокроте нередко обнаруживаются кровянистые прожилки.
При поражении большой части легочной ткани, сдавливании или закупорке бронхиального просвета происходит накопление злокачественного плеврального выпота (метастатический плеврит). У больного появляется одышка, интенсивность которой зависит от объема патологической жидкости.
Иногда температура тела повышается до субфебрильных отметок (37-38 °C) и держится так на протяжении длительного времени.
Рак лёгкого и пневмония
Не столь часто, но всё же приходится проводить в клинической практике дифференциальную диагностику периферического рака лёгких и очаговой пневмонии. Для воспалительного процесса лёгочной ткани инфекционного генеза характерны следующие признаки:
- Пневмония чаще встречается у пациентов моложе 50 лет (хотя может возникнуть в любом возрасте).
- Нет особых различий по полу пациентов (при раке — больше мужчины-курильщики).
- Начало болезни в большинстве случаев острое, с фебрильной лихорадкой.
- Одышка может отсутствовать, но при обширных поражениях лёгочной ткани появляется почти всегда (при онкологии — в далеко запущенных случаях).
- Боли могут возникать при вовлечении плевры.
- Ярко выраженные изменения в результате применения физикальных методов диагностики. Особенно изменяется дыхание, сначала оно становится жёсткое, затем появляются сухие и влажные хрипы.
- При проведении общего анализа крови можно выявить характерные признаки воспаления (рак в данном случае может характеризоваться высоким СОЭ при нормальном содержании лейкоцитов).
- На рентгенологическом снимке видны очаги воспаления гомогенной плотности, чаще — в нижних долях, с расплывчатыми границами, с усилением легочного рисунка и увеличением корней лёгкого.
Патоморфология метастатических узлов
Метастатические узлы, формирующиеся в легких, по своей плотности являются практически полным отражением первичного злокачественного новообразования. Раковые клетки, доставленные в легочную ткань с током крови или лимфатической жидкости, образуют различные по форме метастазы.
По локализации метастатические узлы бывают одно- и двусторонними, а по количеству — солитарными (одиночные периферические новообразования), единичными (2-3 узла) и множественными (более 3 очагов).
В зависимости от эффективности лечебного воздействия при лечении первичного рака, метастазы в легких подразделяются:
- на чувствительные к лучевой и химиотерапии (отсевы хориокарциномы, остеосаркомы, рака яичника, яичка);
- частично поддающиеся консервативной терапии (вторичные очаги немелкоклеточного рака легкого и молочной железы);
- резистентные к облучению и химиотерапии (отсевы меланомы, рака шейки матки, эндометрия, толстой кишки, рака почки).
Какие патологии имеют симптомы, схожие с метастазами в легкие
Рак легкого
— Солитарный узел
— Неправильная форма
— Размытые границы
— Плевральные спикулы
Грибковая инфекция
-Увеличение размеров очагов поражения более быстрыми темпами
— Нечеткие границы
— Фоновое заболевание, предрасполагающее к развитию оппортунистической инфекции
Ревматоидные узелки
— Обычно солитарные
— Известно заболевание, которое явилось причиной образования узелков
Первичная легочная лимфома
— Встречается редко
— Морфологически неразличимы
Диагностика легочных метастазов
В связи с тем, что метастатические узлы чаще всего локализуются в периферических отделах легких, их выявление представляет собой достаточно сложную задачу. Комплексная диагностика легочных метастазов включает в себя следующие методики:
- Обзорная рентгенография легких в прямой и боковой проекции. Проводится для уточнения локализации и протяженности опухоли, ее взаимодействия с корнем легкого и органами, находящимися в средостении.
- Компьютерная томография органов грудной клетки с внутривенным контрастированием. Методика дает возможность определения состояния легочного корня, уточнения характера метастатического процесса, обнаружения мелких очагов диаметром до 10 мм и пораженных внутригрудных лимфатических узлов.
- МРТ. Магнитно-резонансная томография позволяет получить срезы паренхимы легких для выявления структурных изменений и точной локализации опухоли. Но данный метод мало информативен при поражении легких.
- ПЭТ-КТ (позитронно-эмиссионная томография). Используется для измерения метаболической активности тканей легкого. Позволяет выявлять активные метастатические опухоли в легких и других органах. Является наиболее информативным методом оценки метастатического распространения.
- Фибробронхоскопия. Эта эндоскопическая методика предоставляет возможность оценить состояние внутренней поверхности бронхов и взять биопсийный образец опухоли для постановки максимально точного диагноза.
- Тонкоигольная аспирационная биопсия. Назначается при подозрении на формирование опухоли в периферических отделах легкого. Выполняется под контролем рентгенологической аппаратуры.
- Торакоцентез (плевральная пункция). Проводится при наличии плеврального выпота (если злокачественная опухоль затрагивает плевру).
Вторичные образования подразделяются
• диффузно-лимфатические; • узловатые; • смешанные.
Узловая форма — солитарные образования, округлые узлы с четкими контурами, которые располагаются в основном в базальном отделе. По скорости разрастания и характеристикам развития имеют сходство с первичной опухолью. Очаговая форма — мелкие очаги находят совместно с лимфангитом близлежащих тканей легкого, и клиническая симптоматика (сухой кашель, одышка и общая слабость) наблюдается уже на ранних сроках. Диффузно-лимфатический вид — выявляет себя изменениями тяжевого рисунка, что на рентгене будет представлено в виде тонких линейных уплотнений. Распространение злокачественного процесса способствует разрастанию опухолевых теней. Таким пациентам ставят 4 стадию. Плевральная форма — похожи на с экссудативный плеврит — на рентгенограмме выявляются напластования бугристого типа и наличие значительного выпота. Злокачественные процессы плевры сопровождаются ухудшением самочувствия, легочной недостаточностью и температурой субфебрильного вида. Смешанная форма — кроме поражения узлов проявляется лимфангитом и выпотом зоны плевры. В патологический процесс нередко вовлечены медиастинальные узлы. Данные образования называют легочно-плевральными.
Для консультации по методам терапии необходимо предоставить следующие документы: выписной эпикриз, результаты гистологического обследования, заключение КТ или МРТ, информацию о проводимом ранее лечении (если проводилось).
Лечение метастазов
Еще не так давно при выявлении метастатического процесса в легких проводилась только симптоматическая терапия, призванная облегчить состояние пациента. Однако с внедрением инновационного оборудования и новых, более эффективных лечебно-диагностических методик у онкологов появилось больше возможностей для радикального уничтожения вторичных опухолей.
Лечение метастазов в легких назначается с учетом гистологического типа новообразования, возраста и общего состояния больного, а также наличия у него сопутствующих заболеваний. Для повышения эффективности терапии и снижения риска развития осложнений курящим пациентам настоятельно рекомендуется отказаться от курения.
В настоящее время в клинической практике применяются следующие способы борьбы с метастазами в легких.
Хирургическое удаление
Классическое хирургическое лечение метастазов в легких проводится только после резекции первичной опухоли (или при возможности ее полного удаления). Операция выполняется при ограниченном количестве локализованных узлов, их доступности для хирурга, отсутствии отсевов раковых клеток в других органах и абсолютной уверенности в том, что пациент перенесет планируемое лечение.
Лазерная резекция
Вид лечения чаще используемый для реканализации (восстановления проходимости) бронха с просветом, перекрытым опухолью.
Химиотерапия
Это основной вид лечения при множественных метастазах в легких. При разработке схемы химиотерапевтического лечения учитывается характер и распространенность первичной опухоли.
Лучевая терапия
Назначается как при единичных очагах, так и при множественных (в редких случаях). Возможность применения определяется морфологическим видом первичной опухоли, ее чувствительностью к лучевому воздействию, локализацией и размерами очага.
Гормональная терапия
Применение гормональных препаратов является целесообразным при метастатическом распространении гормонально-позитивного рака. Цель данной методики — воздействие на уровень гормонов, способных стимулировать рост злокачественных опухолей.
Радиохирургия
На сегодняшний день одним из самых прогрессивных методов неинвазивного воздействия на единичные метастазы в легких является стереотаксическая радиохирургия. При проведении лечения применяется радиохирургический комплекс «Кибер-Нож», подвергающий опухоль высокоточному, высокоинтенсивному облучению.
Использующая сложное программное обеспечение система состоит из специализированного линейного ускорителя, установленного на роботизированный манипулятор. Он способен двигаться в 6 направлениях, что обеспечивает исключительную гибкость, маневренность и точность. Направленное использование пучков фотонного излучения «Кибер-Ножа» может избавить пациента от метастатического очага без длительного облучения и применения хирургических вмешательств.
Дифференциальная диагностика одиночных очагов в легких
И.Е. Тюрин, д.м.н., зав. кафедрой лучевой диагностики, лучевой терапии и медицинской физики РМАПО (Москва)
Одиночный очаг в легких (ООЛ) представляет собой относительно частый рентгенологический синдром. В отечественной и зарубежной литературе термин очаг определяется различно. Такие изменения представляют собой локальный участок уплотнения легочной ткани округлой или близкой к ней формы диаметром до 3 см, окруженный со всех сторон легочной тканью. Это международное определение несколько отличается от традиционного отечественного представления о легочных очагах, источником которого является фтизиатрическая практика. В классификации туберкулеза размеры очагов не превышают 1 см, а все уплотнения большего размера определяются как инфильтраты, туберкулемы и другие виды изменений. Максимальный размер одиночного очага, равный 3 см, соответствует принятой в настоящее время схеме стадирования немелкоклеточного рака легкого, в которой очаги такой величины относят к Т1 стадии опухолевого роста. Очаги в легочной ткани могут быть одиночными, единичными, в количестве от 2 до 6 включительно, и множественными. Последние относятся к рентгеновскому синдрому диссеминации. Обычно они рассматриваются в контексте дифференциальной диагностики интерстициальных (диффузных паренхиматозных) заболеваний легких. Основной задачей лучевого исследования является неинвазивная дифференциальная диагностика злокачественного и доброкачественного процесса, а также выделение среди них отдельных форм туберкулеза легких. В ряде случаев это возможно на основании характерных симптомов, выявляемых при рентгенографии или рутинной компьютерной томографии (КТ). Тем не менее, специфичность большинства этих признаков низка, поэтому для правильной оценки ООЛ необходимо привлечение дополнительных методических приемов и альтернативных технологий. К ним можно отнести оценку скорости роста очага в легком, анализ вероятностных факторов злокачественности [7], динамика накопления контрастного вещества при КТ и 18фтордеоксиглюкозы (18FFDG) при ПЭТ исследованиях, а также морфологическая оценка изменений по результатам трансторакальной игловой аспирационной биопсии или видеоторакоскопии (ВТС). Очевидно, что единый алгоритм дифференциальной диагностики, предназначенный для всех пациентов и для всех клинических ситуаций, вряд ли может существовать в клинической практике. Задачей любых клинических рекомендаций является точная оценка возможностей отдельных диагностических методов и их сочетаний. Выявление До настоящего времени методом первичного выявления очагов в легочной ткани остается обычное рентгеновское исследование в виде рентгенографии или флюорографии. Одиночные очаги отмечаются в 0,2–1,0% от всех рентгеновских исследований грудной клетки. На обзорных рентгенограммах или флюорограммах редко можно выявить одиночный очаг размером менее 1 см. Даже более крупные очаги могут быть пропущены изза интерпозиции анатомических структур (сердечная тень, корни легких, ребра и др.) или наличия так называемых отвлекающих факторов, например, аномалии развития или патологии сердца. Все большее значение в диагностике легочных очагов приобретает КТ, которое может быть проведена как в случаях подозрения на наличие ООЛ по данным рентгенографии, так и другим причинам, например, исключение пневмонии, ТЭЛА, оценка больных с ХОБЛ и эмфиземой и т.п. В целом, КТ позволяет выявить в 2–4 раза больше очагов в легочной ткани, чем рентгенография, при этом средний размер выявляемых очагов в два раз меньше. Тем не менее, КТ также не является абсолютным методом диагностики. Результаты скрининга рака легкого с помощью низкодозной КТ показывают, что основными причинами пропуска патологии являются небольшие размеры очагов, низкая плотность очагов по типу матового стекла и их локализация в центральных зонах легкого. Анатомическая оценка Оценка скиалогических особенностей одиночного очага по данным рентгенографии или КТ имеет большое значение в дифференциальной диагностике. Очаги можно разделить по размерам, характеру контуров, структуре, плотности, состоянию окружающей легочной ткани. Практически все признаки имеют вероятностное значение. т.е. более или менее характерны для доброкачественного или злокачественного процесса. Лишь в исключительных случаях на основании данных лучевого исследования можно предположить нозологический диагноз. Так, наличие жировых включений типично для гамартомы, кольцевидное или тотальное обызвествление очага обычно наблюдается при туберкулемах, наличие приводящего и отводящего сосуда нарду с типичным усилением при контрастировании отличает артериовенозные мальформации. Локализация очага в легочной ткани не имеет принципиального значения, так как исключения и совпадения наблюдаются здесь слишком часто. Известно, что более 70% одиночных очагов при периферическом раке легкого расположено в верхних долях легких, причем чаще в правом легком, чем в левом. Эта локализация типична и для большинства туберкулезных инфильтратов. Нижнедолевая локализация характерна для рака легкого, возникающего на фоне идиопатического легочного фиброза. Туберкулезные инфильтраты, расположенные в нижних долях, чаще локализуются в верхушечных их сегментах. Очаги в легочной ткани могут иметь различные контуры, в том числе ровные или неровные (волнистые, бугристые), а также четкие или нечеткие (лучистые или размытые за счет зоны матового стекла по периферии). В целом нечеткие и неровные контуры более характерные для злокачественных новообразований, хотя могут наблюдаться и при воспалительных инфильтратах. При размерах очага более 1 см такие контуры являются веским аргументом в пользу наличия злокачественно процесса и, следовательно, показанием для морфологической верификации процесса (рис. 1). Четкие ровные контуры могут наблюдаться при доброкачественных заболеваниях, но постоянно наблюдаются при одиночных метастазах, отдельных гистологических формах рака легкого (плоскоклеточный, мелкоклеточный) и легочных карциноидах. Поэтому округлая форма и четкие контуры очага сами по себе не являются признаками доброкачественности процесса и не могут служить причиной завершения процесса дифференциальной диагностики. Плотность ООЛ, определяемая при КТ, позволяет разделить все очаги на три группы: очаги по типу матового стекла, смешанные или частично солидные очаги, и очаги солидного типа. Очаги по типу матового стекла отличаются низкой плотностью, на их фоне видны стенки бронхов, контуры сосудов и элементы измененного легочного интерстиция. Они наблюдаются при недеструктивных воспалительных процессах, атипичной аденоматозной гиперплазии и при высокодифференцированных аденокарциномах. Очаги смешанного или частично солидного типа характеризуются наличием более плотного участка в центре и зоны низкой плотности по типу матового стекла по периферии. Такие очаги обычно возникают вокруг старых рубцов в легочной ткани, в том числе и посттуберкулезных. В большинстве случаев они представляют собой разрастание железистой опухоли. Солидные очаги имеют типичную структуру локального уплотнения округлой формы мягкотканой плотности с различными контурами, которая может наблюдаться практически при любом патологическом процессе в легочной ткани. Структура ООЛ, выявляемая при КТ, может быть различной: однородной, с участками низкой плотности, обусловленными некрозом, с воздушными, жировыми, жидкостными и высокоплотными включениями, с видимыми просветами бронхов. Ни одни из этих симптомов не является специфичным для какоголибо конкретного патологического процесса, за исключением уже упоминавшихся жировых включений при гамартомах. При рентгеновском исследовании удается выявить лишь часть обызвествлений и включения воздуха в виде полостей, воздушных ячеек (син.: сот, пор), наблюдающихся, например, при железистых карциномах, или просветов бронхов. Обызвествления в ООЛ выявляются при КТ в два раза чаще, чем при обычном рентгеновском исследовании (рис. 2). Обызвествления могут быть очаговыми (по типу воздушной кукурузы), слоистыми, в том числе и виде обызвествления капсулы очага, и диффузными, занимающими весь объем очага (рис. 3). Такие обызвествления типичны для доброкачественных процессов. Исключения составляют лишь метастазы костных сарком, метастатические очаги железистого рака толстой кишки и яичников после химиотерапии и легочные карциноиды. Во всех остальных случаях вероятность неопухолевого процесса исключительно велика. В злокачественных очагах, в том числе в железистых карциномах, нередко выявляют точечные или аморфные, без четких контуров, включения кальция. В целом, частота обызвествлений в периферических раковых опухолях по данным КТ достигает 10%, однако в очагах менее 2 см в диаметре этот показатель обычно не превышает 2%. Такие изменения видны только при высокоразрешающей КТ и не являются дифференциальнодиагностическим признаком, так как могут обнаруживаться и в доброкачественных образованиях. Включения жира обычно наблюдаются при гамартомах (рис. 4). Участки жировой плотности могут выявляться и при первичных липомах, исключительно редких, а также в метастазах липосарком и железистых опухолей почек. При отсутствии внелегочной злокачественной опухоли, наличие жира в легочном очаге является почти патогномоничным признаком гамартомы. Оценка скорости роста Сравнение размеров ООЛ на выполненных предшествующих снимках имеет огромное значение в дифференциальной диагностике. Это сравнение может быть проведено по любым изображениям – флюорограммам, рентгенограммам, линейным или компьютерным томограммам. Отсутствие увеличения очага в течение двух и более лет является одним из надежных признаков доброкачественной его природы. Значительная часть очагов в легочной ткани пропускается при любом первичном исследовании изза скиалогических особенностей патологии или психофизиологических факторов восприятия изображения. Поэтому анализ предшествующих снимков является первым и обязательным этапом дифференциальной диагностики любого ООЛ, а наличие архива изображений (например, флюорографического) значительно повышает эффективность лучевого исследования. Очевидно, что злокачественные опухоли увеличиваются в размерах с большей или меньшей скоростью, что получает отображение на снимках. Время удвоения опухолей колеблется в широких пределах, от 40 до 720 дней. Поэтому появление нового очага в легочной ткани в течение месяца или очаг с неизменными в течение двух и более лет размерами вряд ли представляет собой злокачественную опухоль за исключением очагов по типу матового стекла, которые представляют высокодифференцированную аденокарциному. Пациенты с такого рода очагами требуют более длительного наблюдения. Другим фактором, ограничивающим возможности динамического или ретроспективного наблюдения, являются размеры очага мене 1 см. Удвоение объема опухолевого очага размером 5 мм приводит к увеличению его диаметра на 1.5 мм, до 6,5 мм. Оценка такой динамики находится за пределами возможностей не только традиционной рентгенографии, но и. в большинстве случаев, КТ. В связи этим, большое значение сегодня придается компьютерной оценке объема очагов по данным спиральной КТ, когда ЭВМ строит трехмерные модели выявленных очагов и сравнивает изменение их объема. Эта методика, являющаяся составной частью CAD систем, рассчитана на солидные очаги и не может с уверенностью использоваться для очагов по типу матового стекла и очагов частично солидного типа. Характеристика очагов при динамической КТ Оценка кровоснабжения ООЛ при динамической КТ показала свою эффективность в многочисленных исследованиях. Известно, что плотность очага в легочной ткани при нативном исследовании колеблется в широких пределах и не имеет какоголибо диагностического значения (кроме включений жира и кальция). Смысл динамической КТ заключается в том, что при внутривенном введении контрастного вещества в виде болюса объемом 100 мл патологические образования, имеющие собственную сосудистую сеть, активно его накапливают, при этом плотность их повышается (рис. 5). Типичным примером таких очагов являются злокачественные опухоли. Наоборот, образования, лишенные собственных сосудов, или заполненные бессосудистым содержимым (гной, казеоз, экссудат и т.п.) не изменяют свою плотность. Такие очаги могут быть представлены туберкулемами, кистами, абсцессами и другими патологическими процессами. Наибольшее значение методика динамической КТ при ООЛ имеет в регионах с высокой заболеваемостью туберкулезом, поскольку позволяет точно разделить злокачественные опухоли от туберкулем. Динамическая КТ выполняется в виде серии томографических срезов через патологическое образование, которые выполняются до введения контрастного вещества, во время его введения, через 1, 2, 3 и 4 минуты после введения. Для разграничения доброкачественных и злокачественных процессов необходимо выбрать так называемый порог усиления, т.е. числовое значение коэффициента ослабления, превышение которого позволяет предположить наличие злокачественной опухоли. Начиная с 2000 г. таким порогом, определенным эмпирически в крупном многоцентровом исследовании, является 15 HU. Несмотря на высокую чувствительность в отношении злокачественных опухолей, методика имеет ряд недостатков. К ним относят трудности оценки небольших, менее 1 см, очагов, низкую специфичность, технические ошибки, связанные с дыханием пациента и артефактами от костных структур и контрастного вещества. Эти недостатки частично компенсированы внедрением в клиническую практику многослойной КТ (МСКТ). Кроме того, в большинстве исследований проводиться оценка накопления, но не выведения контраста из очагов. Метаболическая характеристика ООЛ при 18FФДГ ПЭТ Все методы анатомической визуализации, включая рентгеновский, ультразвуковой, КТ или МРТ ориентированы на макроскопические признаки легочных очагов, большинство из которых недостаточно специфичны. В последние года все большее распространение получают исследования возможностей метаболических характеристик очага с помощью 18FФДГ ПЭТ. Известно, что злокачественные опухоли отличаются более высокой метаболической активностью, что характеризуется быстрым и значительным накоплением 18FФДГ в очаге и длительным ее сохранением. Многочисленные исследования показали, что метод отличает высокая чувствительность но относительно низкая специфичность в отношении злокачественных очагов в легких. Более высокие результаты получают при сочетанном использовании ПЭТ и КТ сканеров, так называемые ПЭТ/КТ исследования с последующим совмещением метаболической и анатомической картины. Ложноположительные результаты наблюдаются при активных воспалительных процессах, в том числе при активном туберкулезе легких. Отрицательный результат ПЭТ исследования считается исключительно важным в исключении злокачественной природы легочного очага. Ложно отрицательные заключения могут наблюдаться при первичных опухолях легких по типу матового стекла и при наличии очагов размером менее 7 мм. В этой связи, данные ПЭТ должны обязательно сопоставляться с результатами КТ исследования для более точного понимания их клинического значения. В целом, следует признать, что в настоящее время ПЭТ исследование является наиболее точным методом разграничения доброкачественных и злокачественных очагов в легочной ткани размером более 1 см. Биопсия Для очагов, имеющих анатомические или метаболические признаки злокачественности, необходима морфологическая верификация до начала какоголибо лечения. Это правило обязательно, поскольку тактика обследования и лечения в отношении первичной немелкоклеточной, мелкоклеточной и метастатической опухоли в легком может быть различной. Существует несколько методов забора материала из легочного очага, в том числе трансторакальная игловая аспирация и биопсия, трансбронхиальная биопсия, ВТС резекция очага с последующей биопсией, открытая биопсия при торакотомии. Трансторакальная биопсия проводится под контролем рентгеноскопии, КТ, а в последние годы все чаще при КТ флюороскопии. Трансбронхиальная биопсия обычно выполняется под контролем рентгеноскопии. Пункция очагов, прилежащих к грудной стенке, может быть выполнена с помощью ультразвукового наведения. Транбронхиальная биопсия может выполняться при локализации очага в прикорневых отделах, особенно в случаях, так называемой, централизации злокачественной опухоли. При этом эндобронхиальный компонент может быть выявлен при бронхологическом исследовании. Другим вариантом верификации является браш биопсия, при которой материал забирается с внутренней поверхности бронха, расположенного рядом с очагом или внутри него. Для проведения такой процедуры обязательным является предварительная оценка очага и прилежащих к нему бронхов при высокоразрешающей КТ. Алгоритмы диагностики В настоящее время не существует единого подхода к определению характера ООЛ. Очевидно, что для пациентов с высоким риском злокачественной опухоли оптимальным подходом является наиболее ранняя морфологическая верификация при трансторакальной биопсии. Для пациентов с низким риском злокачественного процесса более рациональным является наблюдение и оценка динамики. В любом случае, современный подход требует выполнения КТ в случаях обнаружения ООЛ при рентгенографии, флюорографии или обычного КТ исследования. Вторым обязательным действием является поиск и изучения любых предшествующих снимков легких. Результатом этих действий может быть выделение группы пациентов с очевидно доброкачественным процессом: отсутствие динамики на протяжении более чем 2 года, наличие «доброкачественных» обызвествлений, включений жира (гамартома), жидкости (киста) в очаге по данным КТ, для которых необходимо только наблюдение. Сюда же относятся выявление АВ мальформации и других сосудистых изменений, случаи воспалительных процессов легких, таких как округлый туберкулезный инфильтрат, туберкулема, мицетома и другие, требующие специфического лечения. Вторым возможным результатом является выявление признаков злокачественного процесса: очаг более 1 см с лучистыми неровными контурами, очаги по типу матового стекла и смешанного солидного типа, которые должны расцениваться как потенциально злокачественные, и для которых необходима морфологическая верификация в условиях специализированного лечебного учреждения. Все остальные очаги определяются как промежуточные или неопределенные. Наиболее многочисленную группу среди них составляют впервые выявленные очаги размером более 10 мм мягкотканой плотности, с относительно четкими ровными или волнистыми контурами, без каких либо включений по данным КТ и без предшествующего рентгеновского архива. Уточнение природы очага в легочной ткани у таких пациентов может осуществляться с помощью биопсии, динамической КТ, ПЭТ и ПЭТ/КТ исследования. Выжидательная тактика и проспективное динамическое наблюдение допустимо здесь лишь в исключительных случаях, обоснованных клинической целесообразностью. Отдельную группу составляют пациенты с выявленными при КТ некальцинированными очагами размером менее 10 мм. Обычно такие очаги обнаруживают при КТ исследовании легких в различных клинических ситуациях, например, исключение пневмонии или ТЭЛА, уточнение характера эмфиземы, трудности интерпретации рентгеновских снимков и т.п. Такие очаги обычно не видны при обычном рентгеновском исследовании, их верификация с помощью трансторакальной биопсии малоэффективна, использование ПЭТ исследования сопряжено с большим количеством ложноотрицательных результатов. Помимо этого, вероятность злокачественного процесса при очагах менее 5 мм не превышает 2%. В связи с этим принята следующая тактика. Очаги размером менее 5 мм не требуют никакого динамического наблюдения. Таким пациентам может быть рекомендовано обычное проверочное исследование (ФЛГ или КТ) через год. Очаги размером 5–10 мм требуют контрольного КТ исследования с интервалом 3, 6, 12 и 24 месяца. В случае отсутствия динамики наблюдение прекращается. Любые изменения формы, размеров, количество очагов является показанием для биопсии. Таким образом, дифференциальная диагностика ООЛ является сложной клинической задачей, которая в современных условиях решается с помощью различных методов лучевой и инструментальной диагностики.
журнал «Поликлиника» 3(1) 2014 стр.28
Диагностика и лечение в «ПЭТ-Технолоджи»
Федеральная сеть центров ядерной медицины «ПЭТ-Технолоджи» имеет огромный опыт проведения ПЭТ-КТ-сканирования и радиохирургических операций с применением системы «Кибер-Нож». У нас можно пройти раннюю диагностику онкозаболеваний и специализированный курс лечения многих первичных опухолей и метастазов. Также для подтверждения или опровержения вызывающего сомнение диагноза «ПЭТ-Технолоджи» предлагает своим пациентам воспользоваться и получить экспертное заключение наших онкологов.
действуют в нескольких регионах России. Для получения онлайн-консультации и записи на прием вы можете связаться с нашим оператором по контактному номеру, использовать форму на сайте или заказать обратный звонок.
Рак лёгкого и инородное тело в бронхах
Во многих случаях аспирация инородного тела в бронх проходит для взрослых незаметно. В таких ситуациях больные могут долго и безуспешно лечиться по поводу рака бронхов или лёгких. После попадания инородного тела, в большинстве случаев возникает судорожный кашель, который может пройти. Фруктовые косточки, семечки, кусочки пластмасс при нахождении в бронхах покрываются грануляцией, которая вызывает хронический воспалительный процесс. Вялотекущее воспаление в данном случае сопровождается периодическим подъёмом температуры, кашлем, сопровождающимся выделением слизистой или слизисто-гнойной мокротой, небольшой одышкой и болью в груди без чёткой локализации.
На рентгенограмме довольно чётко определяется металлическое инородное тело. В противном случае можно лишь различить неясное затемнение поражённого бронха и участок воспаления вокруг него. Поможет дифференцировать инородное тело от рака компьютерная томография, особенно если обтурирован крупный сегмент бронха. В таком случае ставится диагноз обструктивного пневмонита и рассматриваются тактики извлечения инородного тела с минимизацией ущерба для слизистой оболочки бронха.
Можно легко спутать с центральным раком лёгкого эндогенный бронхолит, который представляет собой кальцинированную часть лимфатического узла, попавшего в просвет бронха в результате бронхожелезистой перфорации. При наличии бронхолита пациенты предъявляют примерно такие же жалобы, как и при центральном раке. Дифференцировать данные состояния поможет томография, выполненная в двух проекциях.
Диагностическую ценность имеет и проведение бронхоскопии. Если бронхолит крупный, находится в просвете бронхов или частично расположен в стенке, то можно визуализировать и удалить эндогенное инородное тело. Однако если бронхолит образовался много лет назад, и полностью скрыт грануляционой тканью, то его удаление возможно только при разрушении плотной фиброзной оболочки, покрывающей его. Это чревато сильным кровотечением, так как при хирургических манипуляциях есть вероятность повредить относительно крупные бронхиальные сосуды, проходящие прямо в соединительнотканной оболочке.
При случайном обнаружении затемнения и сомнениях в выборе диагноза между центральным раком и бронхолитом имеет смысл провести бронхоскопию с биопсией. Если онкологический диагноз не подтвердился, то при отсутствии жалоб со стороны пациента можно оставить бронхолит и по необходимости проводить противовоспалительную терапию.
Рак лёгкого и сифилис
Легочное сифилитическое поражение встречается в крайне редких случаях, причём период от манифестации заболевания и появления такого осложнения может составлять 8 лет и больше. При наличии солитарной крупной сифилитической гуммы в лёгочной ткани приходится дифференцировать её с раком лёгкого.
Симптоматика болезни часто не соответствует степени поражения лёгких при сифилисе — относительно нормальное общее самочувствие может сочетаться с резко выраженной одышкой. Течение болезни длительное, часто малосимптомное. При сифилисе лёгких будут отсутствовать малые признаки рака, которые часто бывают дополнительным критерием постановки онкологического диагноза. Также следует брать во внимание длительный сифилитический анамнез, особенно если за всё время лечение было нерегулярным и неадекватным.
Сифилитические гуммы небольшого размера (милиарные, от горошины до лесного ореха), локализуются большей частью в средней и нижней долях лёгкого. Образования могут быть негомогенной структуры, распадаться с образованием каверн. Решающее значение в дифференциальной диагностике будут иметь результаты серологических исследований на сифилис и эффект таргетированного лечения препаратами йода и висмута, а также бициллинотерапии.
«Матовое стекло» при аденокарциноме (раке) легкого
По эффекту «матового стекла» на КТ легких определяют злокачественные новообразования — рак легких. Аденокарцинома — самый распространенный вид опухоли; существенным «спусковым механизмом» для ее образования является курение, наследственность, возраст (старше 40 лет).
Опухоль аденокарцинома формируется из клеток железистого эпителия. На томограмме представлена единичным обычно небольшим (от 2 мм) участком уплотнения по типу «матового стекла». В отдельных случаях у пациента наблюдается несколько «матовых стекол» диффузного или диффузно-мозаичного типа. Аденокарцинома представлена различными морфологическими подтипами и требует динамического наблюдения.
Не пытайтесь самостоятельно интерпретировать изображения. Выявить «матовые стекла» и дать им дифференцированную оценку может только профильный врач специалист, прошедший обучение и имеющий соответствующий сертификат.
«Матовое стекло» на КТ при туберкулезе
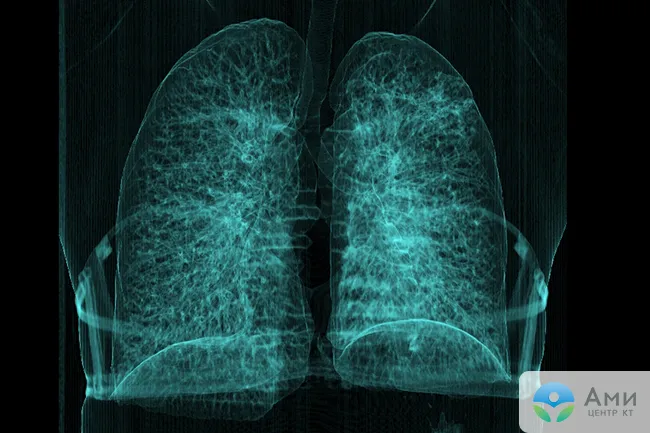
Очаги инфильтрации по типу «матового стекла» встречаются и при туберкулезе. Его вызывает бактерия Mycobacterium tuberculosis. Считается, что все взрослые люди, достигшие возраста 30 лет, являются носителями микобактерии в «спящем» виде. Когда иммунитет подавлен, бактерии туберкулеза могут активизироваться, и человек заболеет.
При туберкулезе на КТ легких обычно видны множественные мелкие (милиарные) очаги, диссеминированные по легким. Возможна их концентрация в определенной доле. Часто присутствует инфильтрат в форме «дорожки», ведущей к корню легкого. Отмечается увеличение лимфатических узлов. Окончательно отличить туберкулез от пневмонии возможно по результатам ПЦР-диагностики — анализа крови на предмет возбудителя инфекционного воспаления легких.