Дефицит железа
5314 29 Января
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Напоминаем вам, что самостоятельная интерпретация результатов недопустима, приведенная ниже информация носит исключительно справочный характер
Гемоглобин: показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
В каких случаях назначают исследование
Поводом к назначению анализа являются диагностированные заболевания костного мозга, а также общие симптомы анемии:
- бледность кожных покровов и слизистых оболочек (конъюнктивы, десен, языка);
- неоправданная слабость;
- быстрая утомляемость;
- частый пульс (нехватка кислорода заставляет сердце сильнее качать кровь).
При общем осмотре стоит обратить внимание и на специфические симптомы, характерные для конкретного вида анемии:
- ломкость волос и ногтей (железодефицитная анемия);
- ярко-малиновый язык (В12-дефицитная анемия);
- желтушность кожных покровов и глазных склер (гемолитическая анемия)
Планово анализ на уровень гемоглобина проводят для комплексной оценки состояния при беременности, перед операциями по пересадке костного мозга или вмешательствах, затрагивающих кроветворные органы. Периодического контроля требует гормональная терапия (в первую очередь, препаратами эритропоэтина), а также длительный прием железосодержащих препаратов.
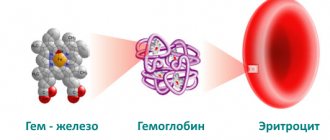
Строение гемоглобина и его структура
Гемоглобин имеет в структуре две части – белок глобин и небелковый гем, строение молекулы позволяет ему присоединять и отдавать кислород, воду и углекислый газ. Гем относится к пигментам, то есть красящим веществам. Он придает крови алый цвет. Внутри гема есть железо. Гемоглобин содержит 4 гема, каждый со всех сторон обвит цепочкой аминокислот белка глобина. Эти 4 субъединицы позволяют связывать 4 молекулы кислорода из воздуха в легких.
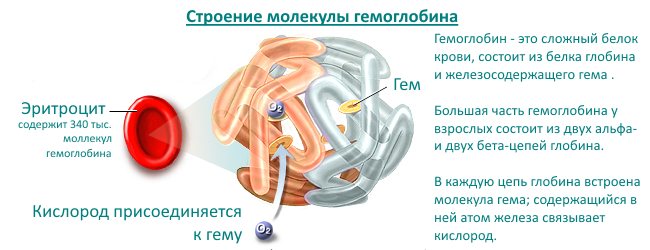
Эритроциты, состоящие на 95% из гемоглобина, захватывают кислородные молекулы и переносят его к клеткам организма. Гемоглобин отдает кислород, а взамен забирает воду и углекислый газ, которые выделяются также через легкие. Соединение гемоглобина с кислородом называется оксигемоглобин, а с углекислотой – дезоксигемоглобин. Все они в норме есть в эритроцитах.
Если гемоглобин соединяется с угарным газом, то блокируются все 4 части молекулы, в результате она теряет способность соединяться с кислородом. Если есть отравление азотом или цианидами, то железо становится из двухвалентного (нормального) трехвалентным. Это тоже нарушает перенос кислородных молекул, образуется метгемоглобин. Подобная реакция бывает и при отравлении некоторыми медикаментами, наследственных болезнях.
Виды
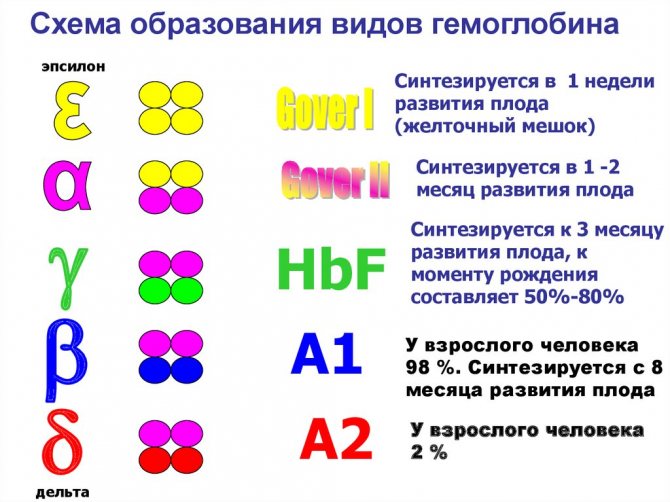
Все виды гемоглобина делятся на нормальные (физиологические) и с нарушенной структурой (патологические). Для их обозначения используют латинские буквы и сокращение Hb (haemoglobinum).
Нормальные формы
В норме можно найти в крови:
- зрелый гемоглобин HbA, его у взрослого 95-98%, а у новорожденного 80%;
- фетальный гемоглобин HbF (фетус означает плод) образуется со 2 месяца беременности у плода, циркулирует до рождения, разрушается в первую неделю жизни, отличается большей способностью захватывать кислород;
- эмбриональный HbE образуется у плода до 2 месяца внутриутробного развития.
В зависимости от того, что присоединил гемоглобин, выделены формы:
- HbО2 – соединение с кислородом (оксигемоглобин);
- HbСО2 – гемоглобин с углекислым газом, он называется дезоксигемоглобин;
- HbMet – метгемоглобин с окисленным железом, его количество в норме допускается до 3%.
Патологические
Патологических гемоглобинов известно более 300 форм. Наиболее часто находят:
- HbS – гемоглобин при серповидно-клеточной анемии;
- HbCO – карбоксигемоглобин, образующийся при отравлении угарным газом;
- HbA1С – гликозилированный гемоглобин, его уровень возрастает при сахарном диабете.
Расшифровка результатов
Для диагностики анемии задействуют общий и/или биохимический анализ крови. По мере необходимости их дополняют другими диагностическими тестами. Особое внимание уделяют следующим показателям:
- уровень гемоглобина (норма: 115-135 г/л – для женщин и 125-145 г/л – для мужчин);
- количество эритроцитов (нормы: 3.7-4.6*1012/л – для женщин и 4.5-5.5*1012 /л – для мужчин);
- насыщенность эритроцитов гемоглобином (норма: 0,8-1,1 ед. – для общего цветового показателя и 28-32 пикограмма – в среднем для каждого эритроцита);
- размер и форма эритроцитов (известно несколько десятков возможных нарушений, в том числе серповидная форма при серповидной анемии или мишеневидная при талассемии);
- уровень клеток-предшественников (ретикулоциты – незрелые эритроциты, слабо насыщенные гемоглобином).
СПРАВКА! Определенный диагностический интерес представляет фетальная форма гемоглобина. В норме она присутствует только у плода и новорожденных детей. По мере развития самостоятельного дыхания и системы кровообращения фетальный гемоглобин заменяется нормальным взрослым (количество фетального гемоглобина в крови не должно превышать 0,5-1,5%).
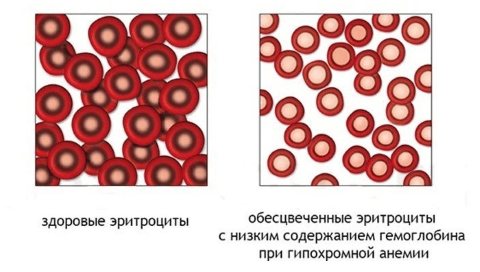
Самый распространенный вариант анемии – железодефицитная. В этом случае проводят анализы на уровень содержания железа:
- сывороточное железо (норма: 11,64–30,43 мкмоль/л – у мужчин, 8,95–30,43 мкмоль/л – у женщин);
- общая железосвязывающая способность сыворотки, ОЖСС (норма: 40,6 – 62,5 мкмоль/л);
- ферритин (белковый комплекс, выполняет роль депо ионов железа);
- трансферрин (транспортный белок) — норма 2,0 – 3,8 г/л для мужчин и 1.85 – 4,05 г/л для женщин.
СПРАВКА! Различные виды отравления влияют на способность гемоглобина переносить кислород, изменяя его структуру (карбоксигемоглобин, метгемоглобин не способны присоединять кислород). Для выявления подобных отклонений используют серию специальных тестов. Специфические формы анализов применяют при подозрении на В12-дефицитную и гемолитическую форму анемии (анализ на аутоиммунные реакции).
Гемоглобин, его функции и физиология
Гемоглобин — сложный белок, хромопротеид, дыхательный пигмент крови человека, позвоночных и некоторых беспозвоночных животных. Основная функция гемоглобина — перенос кислорода от органов дыхания к тканям.
Химически гемоглобин относится к группе хромопротеидов. Молекула гемоглобина состоит из белковой части — глобина и простетичной группы небелковой природы — гема, в состав которого входит железо. В одной молекуле гемоглобина содержится 4 простетических группы. В 100 мл крови здорового человека содержится 13 – 16 г гемоглобина. Железо, которое содержится в геме, способно образовывать с молекулами кислорода распадающееся соединение при прохождении эритроцита через капилляры легких, а при прохождении через сосуды других органов — отдавать кислород и связываться с углекислотой, которую гем затем отдает, когда эритроцит вновь попадает в капилляры легких. Кровь, протекающая по артериям, насыщена кислородом, имеет ярко-алый цвет; после поглощения кислорода тканями и связывания гемоглобина с углекислотой кровь приобретает темно-красный цвет (эта кровь протекает по венам). Помимо гемоглобина крови, у ряда животных в ритмически работающих мышцах с интенсивным обменном (мышца сердца) имеется мышечный гемоглобин (миоглобин), близкий по своему составу и свойствам к гемоглобину крови.
Альфа-полипептидная цепь заканчивается комбинацией аминокислот валина-лейцина, а бета- полипептидная цепь — комбинацией валина-гистидина-лейцина. Альфа- и бета-полипептидные цепи в гемоглобиновой молекуле не размещены линейно, это первичная структура. По причине существования интрамолекулярных сил полипептидные цепи скручиваются в форме типичной для белков альфа-геликсовой спирали (вторичная структура). Сама альфа-геликсовая спираль на каждую альфа- и бета-полипептидную цепь огибается пространственно, образуя сплетения овоидной формы (третичная структура). Отдельные части альфа-геликсовых спиралей полипептидных цепей отмечают латинскими буквами от А до Н. Все четыре третично изогнутые альфа- и бета-полипептидные цепи располагаются пространственно в определенном соотношении — кватернерная структура. Они связаны между собой не настоящими химическими связями, а межмолекулярными силами.
Сведберговой единицей называется комплекс, составленный из одного гема и одной альфа-, бета-полипептидной цепи. Явно гемоглобиновая молекула состоит из четырех сведберговых единиц. Молекулярный вес гемоглобина равен 64458, т. е. на один атом железа полагается по 16115.
Кроме координационной связи, существующей между полипептидными цепями глобина, Fe++ атом гема располагает еще тремя координационными связями, две из которых соединены двумя азотными атомами порфиринового кольца, а третья, в среде с низким парциальным давлением кислорода, связана с одной молекулой воды. В среде с высоким парциальным давлением кислорода (артериальная кровь), третья координационная связь соединена с одной молекулой кислорода, причем получается соединение — оксигемоглобин. Путем непрерывного превращения оксигемоглобина в редуцированный гемоглобин и обратно осуществляется перенос кислорода из легких к тканям. Особенно значительным отличием гемоглобина от миоглобина является кривая насыщения кислородом, которая имеет сигмоидную форму. Значит, возможность гемоглобина связывать кислород зависит от того, заключаются ли в данном тетрамере другие молекулы кислорода. Если содержатся, то последующие молекулы кислорода присоединяются легче. Таким образом, для гемоглобина свойственна кинетика кооперативного связывания, благодаря которой он объединяет максимальное количество кислорода в легких и отдает максимальное количество кислорода при тех парциальных давлениях кислорода, которые имеют место в периферических тканях.
Величина Р50 — значение парциального давления кислорода — характеризует сродство гемоглобинов к кислороду. Р50 у разных организмов существенно различается, но во всех случаях оно превышает значение парциального давления кислорода в периферических тканях рассматриваемого организма.
Это показывает фетальный гемоглобин человека (НВF). Для HbA Р50 26 мм. рт. ст., а для HbF Р50 20 мм. рт. ст. Благодаря этой разнице гемоглобин F отбирает кислород у HbA, находящегося в плацентарной крови. Однако после рождения ребенка HbF утрачивает свою функцию; обладая более высоким сродством к кислороду, он высвобождает меньшее его количество в тканях.
У гемоглобина есть еще одна немаловажная функция: он ускоряет транспорт углекислого газа от тканей к легким. Гемоглобин связывает углекислый газ сразу после высвобождения кислорода; примерно 15% углекислого газа, присутствующего в крови, переносится молекулами гемоглобина. Находящаяся в эритроцитах карбоангидраза катализирует превращение поступающего из тканей углекислого газа в угольную кислоту. Угольная кислота быстро диссоциирует на бикарбонат-ион и протон, причем равновесие сдвинуто в сторону диссоциации. Для предотвращения опасного повышения кислотности крови должна существовать буферная система, способная поглощать избыток протонов. Гемоглобин связывает два протона на каждые четыре освободившиеся молекулы кислорода, определяя буферную емкость крови.
В легких идет противоположный процесс: присоединение кислорода к дезоксигемоглобину сопровождается высвобождением протонов, которые связываются с бикарбонат-ионами, переводя их в угольную кислоту. Далее эффективно действующая карбоангидраза катализирует превращение угольной кислоты в углекислый газ, выдыхаемый из легких. Следовательно, связывание кислорода тесно сопряжено с выдыханием углекислого газа. Это явление называется эффектом Бора.
Этот эффект — свойство тетрамерного гемоглобина, которое определяется гем-гемовым взаимодействием, лежащим в основе кооперативных эффектов. Протоны, ответственные за эффект Бора, высвобождаются в итоге разрушения солевых мостиков, которым сопровождается связывание кислорода с Т-структурой; они отсоединяются от атомов азота остатков гистидина (146) в бета-цепях. Эти протоны сдвигают соотношение в сторону образования угольной кислоты, которая расщепляется карбоангидразой с образованием углекислого газа. Напротив, при высвобождении кислорода вновь складывается Т-структура с присущими ей солевыми мостиками, при создании которых совершается присоединение протонов к остаткам гистидина в бета-цепях. Таким образом, в периферических тканях протоны благоприятствуют образованию солевых мостиков. Образование солевых мостиков вызывает освобождение кислорода из оксигенированной R-формы гемоглобина.
Следовательно, увеличение концентрации протонов содействует освобождению кислорода, а повышение концентрации кислорода стимулирует высвобождение протонов. Первый результат выражается в сдвиге кривой диссоциации кислорода вправо при росте концентрации ионов водорода (протонов).
Обычная концентрация гемоглобина у взрослого человека составляет от 80 до 115%, за среднюю величину принимают 100%. Типичные величины у мужчин приблизительно на 10% выше, чем у женщин. У ребенка же нормальная концентрация гемоглобина существенно отличается от норм взрослого человека.
В наше время существует немало способов нахождения концентрации гемоглобина. Сюда можно отнести колориметрические методы, при которых гемоглобин колориметрируют как оксигемоглобин или редуцированный гемоглобин. К этой группе можно причислить и первый метод для определения гемоглобина, предложенный Велькером в 1854 году и модифицированный Тальквистом, суть которого заключалась в том, что цвет капли крови на фильтровальной бумаге сравнивают с серией цветных бумажных стандартов. Другой исследователь, основываясь на превращении гемоглобина в солянокислый гематин и связанных с этим изменений в электрической проводимости, предложил электронный метод определения концентрации гемоглобина. Также существуют газометрические методы. При этом гемоглобин насыщают газом (например, кислородом), окисью углерода (СО). По доле поглощенного газа определяют количество гемоглобина. Долю кислорода находят прибором Ван-Слайка, прибором Баркрофта или каким нибудь другим аппаратом для определения кислорода. Имеются методы, основанные на определении железа в гемоглобиновой молекуле. Так как гемоглобиновая молекула содержит точно определенное количество железа (0,0347%), по его количеству устанавливается и количество гемоглобина.
Существует такое понятие, как метгемоглобин. Метгемоглобином называется производное гемоглобина, в котором двухвалентный атом железа переходит в трехвалентный. В эритроцитах в ходе обмена всегда формируются известные количества метгемоглобина, который восстанавливается обратно в гемоглобин под влиянием фермента метгемоглобинредуктазы так, что в цельной крови здорового человека метгемоглобин не превышает 2% от общего содержания гемоглобина (0,03 – 0,3%).
Химическая структура сульфогемоглобина не выяснена. Вероятно, две виниловые группы гемоглобина соединяются, посредством SО2-мостиков, с соседними метиновыми связями. В нормальном состоянии сульфогемоглобина в крови нет. Он появляется при отравлениях соединениями сурьмы, фенацитином, бромом, сульфонамидами, нитратами (колодезная вода), серными соединениями и пр.
Определение сульфогемоглобина в крови можно произвести спектроскопически. Сульфогемоглобиновый спектр не изменяется от прибавления сульфида аммония, но исчезает от прибавления Na2S2О4 и 2 мл 10% едкого натра, или нескольких капель 3% перекиси водорода.
Типы гемоглобина. Недавно еще считалось, что гемоглобин взрослого человека представляет собой единственное соединение. Известно было только то, что в эмбриональной жизни имеется особенный тип гемоглобина, называемый HbF, в 155 раз более устойчивый к n/12 натриевой щелочи, чем нормальный гемоглобин. В последнее время, благодаря работам Полинга, его сотрудников и др., выяснилось, что гемоглобин взрослого человека и при нормальных, и при патологических состояниях не представляет собой гомогенного химического соединения. Открыто было много нормальных и патологических типов гемоглобина, которые представили в новом свете обмен гемоглобина и указали пути для исследования патогенеза некоторых анемий. Установлено было, что при некоторых заболеваниях наблюдаются особые типы гемоглобина, характерные для данной анемии. Типы гемоглобина имеют большое значение не только для диагноза, но и переносят вопрос о патогенезе анемии из чисто морфологической области в биохимическую. Анемии, вызванные появлением патологического типа гемоглобина, называются гемоглобинопатиями или гемоглобинозами.
Выяснилось, что у человека имеются три основных типа нормального гемоглобина: эмбриональный — U, фетальный — F и гемоглобин взрослого человека — А. HbU (назван по начальной букве слова uterus) встречается в эмбрионе между 7 и 12 неделями жизни, затем он исчезает и появляется фетальный гемоглобин, который после третьего месяца является основным гемоглобином плода. Вслед за этим появляется постепенно обыкновенный гемоглобин взрослого человека, называемый HbA, по начальной букве английского слова «adult». Количество фетального гемоглобина постепенно уменьшается, так что в момент рождения 80% гемоглобина представляет собой HbA и только 20% — HbF. После рождения фетальный гемоглобин продолжает убывать и к 2 – 3 году жизни составляет всего 1 – 2%. То же количество фетального гемоглобина и у взрослого. Количество HbF, превышающее 2%, считается патологическим для взрослого человека и для детей старше 3 лет.
Кроме нормальных типов гемоглобина, в настоящее время известно свыше 50 его патологических вариантов. Они сначала были названы латинскими буквами. Буква В в обозначениях типов гемоглобина отсутствует, т. к. ею обозначен первоначально HbS.
Вскоре выяснилось, что букв азбуки не хватит для обозначения всех патологических типов гемоглобина. Поэтому стали применять для этого имена пациентов, больниц, лабораторий, названия мест и округов. Самой удобной является номенклатура по структурной формуле.
Как нормальные, так и патологические типы гемоглобина различаются не по структуре протопорфиринового кольца, а по построению глобина. Разница может заключаться в изменении целых пар полипептидных цепей в гемоглобиновой молекуле.
Такая возможность встречается у гемоглобинов H, F, Бартс, А2 и U. Вместо нормальной структуры гемоглобина А — альфа-альфа/бета-бета (альфа 2/бета 2), гемоглобин Н имеет структуру бета-бета-бета-бета (бета 4), что значит, что обе альфа-полипептидные цепи замещены новыми — бета-полипептидными цепями. У гемоглобинов F, Бартс и А2 появляются две новые цепи, обозначаемые гамма и дельта, а у гемоглобина U — новая цепь, обозначаемая ипсилон. Структура HbF — альфа-альфа/гамма-гамма (альфа 2/гамма 2), структура гемоглобина Бартс — гамма-гамма-гамма-гамма (гамма 4), структура HbА2 — альфа-альфа/дельта-дельта (альфа 2/гамма 2), структура гемоглобина U — альфа-альфа/ипсилон-ипсилон (альфа 2/ипсилон 2).
Патологические гемоглобины, которые состоят из четырех одинаковых полипептидных цепей, обозначают тетрамерами. Тетрамеры альфа и дельта до сих пор in vivo не наблюдались.
Существует и другая возможность, которая встречается у большинства типов гемоглобина. Так, например, единственная разница между HbS и HbA состоит в том, что на 6-ом месте в бета полипептидной цепи вместо глутамина находится валин, единственная разница между HbI и HbA в том, что на 16-ом месте в альфа-полипептидной цепи лизин замещен аспарагиновой кислотой.
Когда аномалия состоит в замещении аминокислоты в альфа-полипептидной цепи, то говорят об альфа-аномалии, когда состоит в бета-полипептидной цепи — о бета-цепной аномалии, когда в гамма-полипептидной цепи — о гамма-цепной аномалии (патологические варианты HbF), когда в дельта-цепи — о дельта-цепной аномалии (патологические варианты HbA2).
При изучении гемоглобиновых типов имеет большое значение вопрос о структуре глобинов. С одной стороны, структура является самым верным способом отдифференцирования отдельных типов гемоглобина один от другого, с другой стороны — создается возможность для составления строго научной номенклатуры последних. Методы дифференцировки видов гемоглобина
Для разграничения отдельных типов человеческого гемоглобина пользуются электрофорезом на блоке крахмала, на крахмальном геле, на геле агара, на целлюлозно-ацетатных листах, на акриламидном геле, на карбоксиметилцеллюлозном геле, электрофорезом при высоком напряжении тока.
Вторым по значению методом, которым пользуются в настоящее время для дифференциации отдельных видов гемоглобина, является хроматография.
Особенно хорошие результаты получается при употреблении в качестве адсорбирующего вещества ионообменной смолы амберлита и ионообменного декстранового геля.
Для разграничения некоторых видов гемоглобина пользуются также их растворимостью в некоторых растворителях.
Наиболее известным тестом этой группы является проба Итано для доказательства наличия HbS. При этой пробе редуцированный HbS осаждается в 24 m буфере, в противоположность другим типам гемоглобина. Проба эта имеет особенное значение для дифференцирования HbS и HbD, потому что HbS и HbD обладают одинаковой электрофоретической и хроматографической подвижностью.
Для отличия HbA от HbF пользуются, как было подчеркнуто выше, устойчивостью при денатурации растворами натриевой щелочи. Это известный в истории метод, которым Кербер в 1886 году дифференцировал HbA и HbF.
Гемоглобины группы F отличается от других гемоглобиновых типов и по своей характерной триптофановой полосе при 289,8 нм ультрафиолетового спектра. Гемоглобины, обладающие группой М, не имеют абсорбционной полосы при длине волны 630 нм, но зато показывают увеличенную абсорбцию при 600 нм.
«Отпечатковый метод”. Дело касается важнейшего метода установления «первичной структуры» гемоглобина при различных гемоглобиновых типах. Исследуемый гемоглобин гидролизуют трипсином, при этом полипептидные цепи глобиновой молекулы распадаются на большое число пептидов. Пептидную смесь подвергают электрохроматографии на бумаге, т. е. в одном направлении проводится электрофоретическое, в другом — хроматографическое разделение. Получаются характерные для отдельных типов гемоглобинов электрохроматограммы, по которым их можно точно различить. Определение аминокислотного состава отдельных пептидов дает возможность выявления первичной структуры глобина соответствующего гемоглобинового типа. Проводя аналогию с соответствующей по сложности и точности криминалистической техникой для изучения отпечатков пальцев рук, он был назван «пальцеотпечатковым» («fingerprint») методом.
Так называемым «рекомбинационным» или «гибридизационным» методом можно воспользоваться для установления состава полипептидных цепей в каком-нибудь гемоглобиновом типе. Если смешать известный и неизвестный гемоглобин при рН 4,3, они диссоциируют полумолекулами, состоящими из соответствующих пар полипептидных цепей. Полипептидные пары снова комбинируются в целые гемоглобиновые молекулы после нейтрализации раствора, причем могут получиться и новые «гибридные» гемоглобиновые молекулы. Их идентифицирование электрофоретическим способом или хроматографией позволит сделать заключение о полипептидной структуре неизвестного гемоглобинового типа. Этот метод также предназначен преимущественно для научных исследовательских целей.
Существуют также способы цитологического определения типа гемоглобина в эритроцитах на мазке крови. Присутствие HbF в эритроцитах можно обосновать путем обработки кровяного мазка лимоннокислой буферной смесью с рН 3,2 – 3,6. При этих условиях HbA извлекается, и эритроциты, в которых он преобладал, остаются только в виде эритроцитных теней, тогда как HbF сохраняется, а эритроциты, содержащие преимущественно этот тип гемоглобина, сохраняют свое содержание.
Помимо всех этих методов при дифференциации некоторых типов гемоглобина пользуются также разницей в кристаллическом строении, изоэлектрической точке и т. д.
Рассмотрим гемоглобин S, в котором остаток Glu А2 бета замещен на Val.
Он располагается на поверхности молекулы гемоглобина и контактирует в водой, и замещение полярного остатка Glu на неполярный Val ведет к появлению на поверхности бета-субъеденицы «липкого участка». Этот липкий участок присутствует как в оксигенированном, так и в дезоксигенированном гемоглобине S, но в гемоглобине А отсутствует.
Существует комплементарный участок на поверхности дезоксигенированного гемоглобина, который способен крепко соединяться с липким участком бета-субъединицы, тогда как в оксигенированном гемоглобине этот участок маскируется другими группами. Когда гемоглобин S переходит в дезоксигенированное состояние, его липкий участок связывается с комплементарным участком на другой молекуле дезоксигенированного гемоглобина, тем самым совершается полимеризация дезоксигемоглобина S и его осаждение в виде длинных волокон.
Волокна дезоксигемоглобина S механически деформируют эритроцит, придавая ему серповидную форму, что приводит к лизису клеток и множеству вторичных клинических проявлений.
Следовательно, если бы можно было поддерживать гемоглобин S в оксигенированном состоянии или хотя бы свести к минимуму концентрацию дезоксигенированного гемоглобина S, то удалось бы предотвратить полимеризацию дезоксигенированного гемоглобина S и формирование «серповидных» клеток. Полимеризации подвержена Т-форма гемоглобина S. При серповидноклеточной анемии: гемоглобин S в ферри-состоянии (метгемоглобин S) не подвержен полимеризации, поскольку он стабилизирован в R-форме.
В дезоксигемоглобине А тоже есть рецепторный участок, способный взаимодействовать с липким участком оксигенированного или дезоксигенированного гемоглобина S, но присоединения «липкого» гемоглобина S к дезоксигемоглобину А мало для создания полимера, так как сам дезоксигемоглобин А липкого участка не заключает в себе и не может объединять следующую молекулу гемоглобина.
Значит, связывание дезоксигемоглобина А с R- или Т-формой гемоглобина S перекрывает полимеризацию.
Спиральные фибрилярные структуры формируются в результате полимеризации дезоксигемоглобина S. При этом каждая молекула гемоглобина контактирует с четырьмя соседними молекулами. Создание подобных трубчатых волокон ответственно за механические нарушения в содержащем их эритроците.
Существует еще одна группа патологий — талассемия, которые связанны с аномалиями гемоглобина. В их характеристику входит сниженная скорость синтеза альфа-цепей гемоглобина (альфа-талассемия) или бета-цепей (бета-талассемия). Это приводит к анемии, которая может принимать очень тяжелую форму.
В наше время проводится много исследований, которые позволяют выяснить молекулярные приспособления, отвечающие за развитие талассемии.Гемоглобин — сложный белок в составе эритроцитов, состоящий из 2х частей: белка (глобин) и соединения железа (гема). Именно атомы железа (гема) делает кровь красной.
Гемоглобин участвует в процессе транспорта кислорода и углекислого газа между легкими и клетками других органов, поддерживает рН крови. При недостатке гемоглобина в крови затрудняется перенос кислорода гемоглобином. В результате клетки не получают достаточно кислорода и в них нарушается обмен веществ и функции.
Формы гемоглобина. При присоединении к белку гемоглобина (глобину) глюкозы, образуется гликозилированный (гликированный) гемоглобин.
Рост уровня гликолизированного гемоглобина происходит при переизбытке глюкозы в крови, возникающем при сахарном диабете.
В соответствии с рекомендациями Всемирной Организации Здравоохранения (ВОЗ) анализ на гликозилированный гемоглобин — самый эффективный и необходимый метод в диагностике сахарного диабета. Больным сахарным диабетом рекомендуется сдавать биохимический анализ крови на гликозилированный гемоглобин не реже 1 раза в квартал.
Врачи выделяют еще одну форму гемоглобина — фетальный гемоглобин, отличающийся от нормального гемоглобина по строению и свойствам. Фетальный гемоглобин — это гемоглобин новорожденных, содержание в крови фетального гемоглобина ребенка достигает 80%. К 1 году жизни фетальный гемоглобин у детей начинает разрушаться и практически полностью заменяется на гемоглобин взрослых. Фетальный гемоглобин — норма у детей, но для взрослых его содержание — признак серьезных заболеваний. Определение гемоглобина новорожденных используется в диагностике заболеваний крови и онкологических заболеваний.
Норма гемоглобина
| Норма гемоглобина, г/л | |
| Мужчины | 135—160 |
| Женщины | 120—140 |
Содержание гемоглобина в крови у мужчин выше, чем у женщин. Гемоглобин у ребенка до 1 года понижен.
Норма гликированного гемоглобина — 4—6,5 % от уровня свободного гемоглобина в крови. При чем уровень гликированного гемоглобина может не зависеть от концентрации гемоглобина в крови. Норма гемоглабина новорожденных (фетального гемоглобина) в крови взрослого — до 1%.
Анализ крови на гемоглобин — необходимый этап диагностики различных заболеваний. По результатам только одного анализа крови на гемоглобин невозможно поставить точный диагноз, но определение гемоглобина выявит возможные нарушения в деятельности организма и укажет на необходимость дополнительного обследования.
Повышенный гемоглобин — симптом следующих заболеваний:
· эритроцитоз (заболевание, сопровождающиеся увеличением количества эритроцитов в крови)
· сгущение крови
· врожденные пороки сердца
· кишечная непроходимость
· ожоги
· сердечно-легочная недостаточность.
Высокий уровень гликолизированного гемоглобина — симптом сахарного диабета и дефицита железа.
Повышение гемоглобина в крови происходит после физической нагрузки, у альпинистов, у летчиков — после высотных полетов. Высокий гемоглобин в крови характерен для жителей высокогорья. Повышенный уровень гемоглобина в крови может возникнуть даже после пребывания на свежем воздухе.
Состояние организма, при котором происходит снижение гемоглобина в крови, называется анемией. Анемия может развиться в результате потери гемоглобина при кровотечениях, при заболеваниях крови, сопровождающихся разрушением эритроцитов. Низкий гемоглобин возникает вследствие переливания крови.
Причиной понижения гемоглобина — анемии может стать нехватка железа или витаминов (В12, фолиевой кислоты), необходимых для синтеза гемоглабина и эритроцитов.
Анализ крови на гемоглобин может показать пониженный гемоглобин вследствие различных хронических заболеваний (талассемии и др.).
Снижение уровня гликированного гемоглобина происходит при гипогликемии, гемолитической анемии, кровотечениях и переливании крови.
Зачастую происходит понижение гемоглобина у беременных женщин. При беременности гемоглобин обычно понижается при нехватке железа, поскольку суточная потребность в железе беременных женщин увеличивается. Если обычно человеку достаточно 5—15 мг железа в день, то беременной женщине потребуется 15—18 мг. Врачи рекомендуют беременным женщинам следить за уровнем гемоглабина в крови, поскольку низкий гемоглобин беременных может отрицательно отразиться на здоровье будущей матери, вызвать преждевременные роды или задержку роста плода.
Информация о работе «Гемоглобин, его функции и физиология»
Раздел: Медицина, здоровье Количество знаков с пробелами: 24765 Количество таблиц: 1 Количество изображений: 0
Похожие работы
Физиология
119359
2
0
… ОБЩАЯ ФИЗИОЛОГИЯ ВОЗБУДИМЫХ ТКАНЕЙ (два занятия) Занятие 1-е ПРИРОДА ВОЗБУЖДЕНИЯ 1.Что называют раздражимостью и возбудимостью? 2.Каково соотношение понятий раздражимость и возбудимость? Какие ткани в физиологии называют возбудимыми,какие- невозбудимыми? 3.Клетки каких тканей организма являются возбудимыми и невозбудимыми? 4.Дайте определение понятию «раздражитель». 5.Назовите два вида …
Предмет, задачи и методы возрастной физиологии
179193
1
0
… возрастает. В этом немалую роль играют воспитательные воздействия, направленные на совершенствование внутреннего торможения. Литература 1. Бадалян Л.О. Невропатология. – М.: Академия, 2000. – 384 с. 2. Беляев Н.Г. Возрастная физиология. – Ставрополь: СГУ, 1999. – 103 с. 3. Дубровская Н.В. Психофизиология ребенка. – М.: Владос, 2000. – 200 с. 4. Обреимова Н.И., Петрухин А.С. …
Физиология человека
488745
0
0
… . И.П. Павлову, первому из русских ученых, 7 октября 1904 г. была присуждена Нобелевская премия в знак признания его работ по физиологии пищеварения. Потребность организма в пище проявляется в виде физиологической реакции голода. У человека голод приобретает выраженную субъективную окраску — от относительного безразличия к пище до яркой эмоциональной реакции. Физиологической основой голода …
Оружие геноцида: самоубийство людей и его механизмы
440441
3
7
… в состоянии продолжать жить, несмотря на указания совести о неправильности жизни…». На этом тезисе мы закончили предыдущую главу книги. Не развивая его, поскольку это не входит в достаточно узкую заявленную тематику оружия геноцида, обратимся к внутренним механизмам, которые включаются у людей после принятия психотропов. Мы знаем от чего люди убегают (от своей совести). Но за чем же люди гонятся? …
Биологическая роль гемоглобина
Основная биологическая роль гемоглобина – это обеспечение тканевого дыхания, переноса кислорода для образования энергии и удаления углекислого газа. При этом первая его функция основная для организма, так как без гемоглобина кислородное обеспечение невозможно. Для выведения углекислоты есть и другие пути – 80% ее просто растворяется в крови и только 20% переносит гемоглобин.
Нарушение этих процессов происходит при снижении абсолютного числа гемоглобина или потери его активности. Чтобы проверить достаточность питания клеток кислородом, назначается общий анализ крови, а последствия нехватки показывает биохимия:
- напряжение кислорода;
- кислородная емкость;
- артерио-венозная разница по кислороду;
- насыщение гемоглобина кислородом.
МСНС. Норма
Нормальные значения средней концентрации гемоглобина в эритроците представлены в таблице.
| Возраст, пол | Средняя концентрация гемоглобина в эритроцитах г/дл | |
| 1 – 14 дней | 28 – 35 | |
| 2 – 4,3 недели | 28 – 36 | |
| 4,3 – 8,6 недель | 28 – 35 | |
| 8,6 недель – 4 месяца | 29 – 37 | |
| 4 – 12 месяцев | 32 – 37 | |
| 1 – 3 года | 32 – 38 | |
| 3 года – 12 лет | 32 – 37 | |
| 12 – 15 лет | Ж | 32 – 36 |
| М | 32 – 37 | |
| 15 – 18 лет | Ж | 32 – 36 |
| М | 32 – 36 | |
| 18 – 45 лет | Ж | 32 – 36 |
| М | 32 – 37 | |
| 45 – 65 лет | Ж | 31 – 36 |
| М | 32 – 36 | |
| Старше 65 лет | Ж | 32 – 36 |
| М | 31 – 36 | |
Частые вопросы по структуре гемоглобина
Какая валентность железа в гемоглобине? В норме железо двухвалентное, при окислении переходит в трехвалентное, что ухудшает перенос кислорода.
В чем особенность химического строения гемоглобина? Гемоглобин имеет четвертичную структуру, то есть белковые цепи и пигмент вначале соединены в комплексы (первичная структура), а потом эти четыре субъединицы скрепляются между собой.
Что такое нативный гемоглобин и какую он имеет структуру? Нативный гемоглобин – это нормальный, не поврежденный, в его структуре есть гем и глобин, соединенные в 4 комплекса.
Сколько атомов железа в молекуле гемоглобина? В составе гемоглобина 4 гема с железом, поэтому в одной молекуле содержится 4 атома этого микроэлемента.
Строение гемоглобина позволяет ему присоединить кислород, переносить его к клеткам, забирать углекислый газ. При снижении возникает анемия с симптомами кислородного голодания.