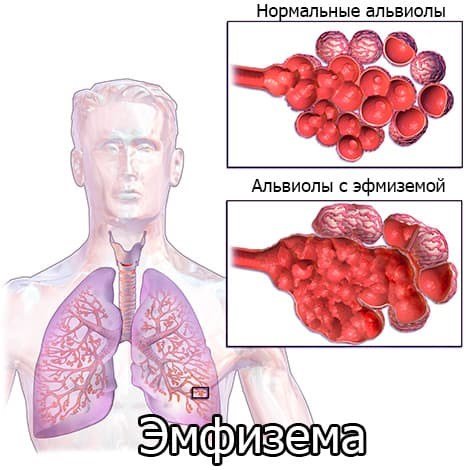
Как развивается эмфизема легких
Что это такое эмфизема легких?
Это стойкое увеличение воздушных пространств легких дистальнее терминальных бронхиол с деструкцией альвеол.
Признаки эмфиземы легких легкой формы обнаруживают на аутопсии в 2/3 случаев.
Основные причины и признаки эмфиземы легких:
- Гипоплазия, обусловленная бронхолегочным заболеванием
- Атрофия, т.е. потеря паренхимы. Данная форма наблюдается, например, у курильщиков (курение — наиболее важный этиологический фактор) и у пожилых людей (старческая эмфизема)
- Повышенная воздушность легких или деструкция периферических дыхательных путей (клапанный механизм, терминальная стадия воспалительных заболеваний, недостаточность a1-антитрипсина).
- Формы:
- Центролобулярная эмфизема (у курильщиков, часто связана с хроническим бронхитом, сопутствующими воспалительными изменениями и фиброзом)
- Панлобулярная эмфизема (недостаточность a1-антитрипсина, синдром Маклеода/Суайра-Джеймса, семейная форма)
- Парасептальная эмфизема.
Коррекция образа жизни больным с эмфиземой
При обнаружении на рентгенограмме стойкой эмфиземы следует скорректировать образ жизни для облегчения общего самочувствия и улучшения качества жизни. Рекомендуются следующие мероприятия:
- Бросить курить, так как табакокурение — главная причина формирования ХОБЛ.
- Сменить трудовую деятельность (если она связана с химической, угольной, мукомольной и другими отраслями, увеличивающими риск развития обструкции и других заболеваний органов дыхания).
- Переехать в экологически чистый регион или хотя бы пролечиваться в санаторных условиях раз в год, климат нужно выбирать сухой и тёплый.
- Соблюдать гипоаллергенную диету, так как иногда продукты питания могут быть причиной бронхиальной астмы и приводят к бронхообструкции.
- При любых заболеваниях верхних дыхательных путей следовать рекомендациям врача, строго соблюдать назначенную терапию.
Эмфизема лёгких — логическое завершение хронического обструктивного процесса. Патология сопровождается значительными изменениями функционального состояния лёгочной ткани, клинически проявляется признаками дыхательной недостаточности.
При прогрессировании и декомпенсации процесса формируются сердечно-сосудистые нарушения. Важно обнаружить первые признаки эмфизематозных изменений для своевременной коррекции образа жизни и профилактики серьёзных осложнений. Альтернативными методиками выступают и МРТ.
Какой метод диагностики эмфиземы легких выбрать: МРТ, КТ, рентген
Метод выбора
- КТ.
Для чего проводят рентген грудной клетки при эмфиземе
- Чувствительность метода низкая и составляет примерно 50% (легкие формы заболевания могут остаться незамеченными)
- Специфичность высокая (>90%)
- Деформация грудной клетки (бочкообразная грудная клетка вследствие увеличения сагиттального размера, широких межреберных промежутков; уплощение реберно-диафрагмальных синусов)
- Низкое стояние и уплощение диафрагмы
- Обеднение периферического легочного сосудистого рисунка
- Расширение сосудов корня легкого
- Повышенная прозрачность легочных полей
- «Эмфизематозное (легочное) сердце».
Что покажет МСКТ грудной клетки при эмфиземе
- Парасептальная эмфиземе легких — буллезная
- Поражаются преимущественно базальные сегменты легкого
- При панлобулярной эмфиземе легких нарушается архитектоника всей дольки
- При центролобулярной эмфиземе легких отмечается деструкция стенки альвеол в центре вторичных легочных долек, периферические отделы долек и сосуды интактны
- Участки повышенной рентгенопрозрачности (эмфиземный порог составляет менее -950 HU; нормальная плотность легочной ткани находится в пределах от -750 до -900 HU).
- Поражаются преимущественно краниальные сегменты легкого.
- Сосудов становится меньше
- Особая форма панлобулярной эмфиземы развивается при недостаточности a1-антитрипсина.
- Преимущественно затрагивает субплевральные и бронховаскулярные участки легкого.
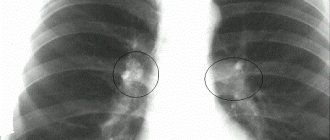
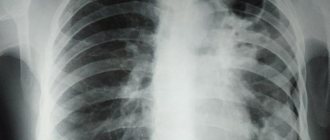
Эмфизема легких у мужчины 50 лет. На обзорной рентгенограмме грудная клетка имеет колоколообразную форму, диафрагма уплощена, уровень стояния ее низкий, сосудистый рисунок легких обеднен. Незначительная изогнутость отдельных сосудов. Тень сердца уменьшена, легочный ствол выбухает.
Специфичные симптомы
- Рентгенография грудной клетки: типичная картина регионарного или глобального повышения прозрачности легочных полей и обеднение периферического сосудистого рисунка
- КТ: деструкция стенки альвеол.
Методы диагностики
Поставить пациенту точный диагноз позволяют:
- рентгенография, на снимке которой в легких заметны прозрачные участки, наполненные воздухом;
- спирометрия, позволяющая уточнить объем вдыхаемого и выдыхаемого воздуха. При эмфиземе второй показатель гораздо больше первого;
- пикфлоуметрия помогает уточнить скорость выдоха при приеме бронхорасширяющих препаратов и без их применения.
Дополнительным методом диагностики эмфиземы легких является анализ крови, по которому можно отследить наличие воспалительного процесса в организме и его интенсивность.
Набор необходимых диагностических мероприятий зависит от состояния конкретного пациента и необходимости в детализации картины его здоровья.
Клинические проявления
Типичные симптомы эмфиземы легких:
- Нарушение дыхания зависит в основном от морфологических изменений и в меньшей степени от типа эмфиземы легких
- Старческая эмфизема легких и повышенная воздушность легких часто протекают бессимптомно
- Симптомы эмфиземы легких у «Розовых пыхтелыциков» — больные, жалующиеся на затрудненное дыхание при физической нагрузке, непродуктивный кашель при относительно нормальном содержании газов в артериальной крови
- У «синих одутловатиков» дыхание нормальное, но поражены бронхи, что проявляется цианозом и хроническим рецидивирующим бронхитом
- Признаки легочной гипертензии
- Увеличены общая емкость легких и остаточный объем; OФB1 и перфузионная способность легких снижены.
Причины развития эмфиземы
Воздействие эндогенных факторов:
- Нарушение микроциркуляции крови в паренхиме легких;
- Изменение морфологии сурфактанта;
- Дефицит A1AT (Альфа-1-антитрипсина);
- Наследственная предрасположенность;
- Заболевания дыхательных путей (особенно хронический бронхит);
- Старение.
Воздействие экзогенных факторов:
- Нарушение микроциркуляции крови в паренхиме легких;
- Изменение морфологии сурфактанта;
- Дефицит A1AT (Альфа-1-антитрипсина);
- Наследственная предрасположенность;
- Заболевания дыхательных путей (особенно хронический бронхит);
- Старение.
Легочная ткань представляет собой эластичный каркас, похожий на губку. Маленькие камеры, которые на вдохе наполняются воздухом, а на выдохе опустошаются – это альвеолы. При эмфиземе мелкопористая губка становится крупнопористой и растягивается, ее волокно теряет прочность и разрушается. Диаметр одних альвеол расширяется, однако другие воздушные камеры разрушаются. Площадь функциональной легочной ткани сокращается, возникают буллы – бесполезные мешкообразные участки легких, которые не участвуют в газообмене. Со временем у пациентов с эмфиземой легких также деформируется грудная клетка – она расширяется и принимает бочкообразную форму.
Течение и прогноз
- Осложнения включают спонтанный пневмоторакс и рецидивирующие бронхолегочные инфекции
- Ограничение функции легких коррелирует со степенью изменений легочной паренхимы
- При далекозашедшей форме заболевания прогноз неблагоприятный.
Для количественной оценки и классификации эмфиземы легких необходима КТ. Центролобулярная эмфизема (а) характеризуется мелкоузелковыми просветлениями, соответствующими раздутым альвеолам в центре ацинусов. Для панлобулярной эмфиземы (с) характерны генерализованная воздушность и деструкция легочной паренхимы. Часто встречаются переходные формы (b) между центролобулярной и панлобулярной эмфиземой. Парасептальная эмфизема наблюдается часто и обычно не имеет клинического значения (d). На представленных томограммах она сочетается с центролобулярной эмфиземой.
Диагностика функциональных нарушений
Выполнение функциональных тестов во время рентгенографии имеет важное значение для дифференциальной диагностики необратимых изменений легочной ткани.
При эмфиземе, несмотря на увеличенный объем, отсутствует функциональный обмен отработанного воздуха. В расширенных альвеолах содержится такой же воздух. Это приводит к снижению оксигенации крови и клиническим признакам гипоксии.
Для определения рентгенологических симптомов необратимых функциональных изменений используются следующие тесты:
- Метод Соколова: делается серия последовательных снимков на разных фазах дыхательного цикла на рентгеновской пленке размером 13×18 см, после чего прогиб диафрагмы сравнивается с линейкой;
- Метод прицельной визуализации — прицельная диагностика области локальной эмфиземы: делается несколько снимков на глубоком вдохе, затем на выдохе, задержке дыхания и затем сравниваются результаты;
- Метод интродьюсера: правое легкое закрывается так, чтобы купол диафрагмы находился ниже нижнего края интродьюсера. Затем делается серия фотографий, на которых расстояние от диска до диафрагмы во время фаз вдоха, выдоха и задержки дыхания определяет степень отклонения легких.
Какие заболевания имеют симптомы, схожие с эмфиземой легких
Легочная киста и другие кистозные поражения
— Структура стенки различима
Бронхиальная астма
— Деструкция паренхимы отсутствует
— Повышенная воздушность может пройти после назначения бронхолитиков
Облитерирующий бронхиолит
— Деструкция паренхимы отсутствует
— Перфузия легочной ткани мозаична
Лимфангиолейомиоматоз
— Встречается почти исключительно у женщин в репродуктивном периоде
— Тонкостенные кисты
— Хилезная плевральная жидкость
Гистиоцитоз X
— Узелковые изменения
Повышение прозрачности на рентгене: что это такое
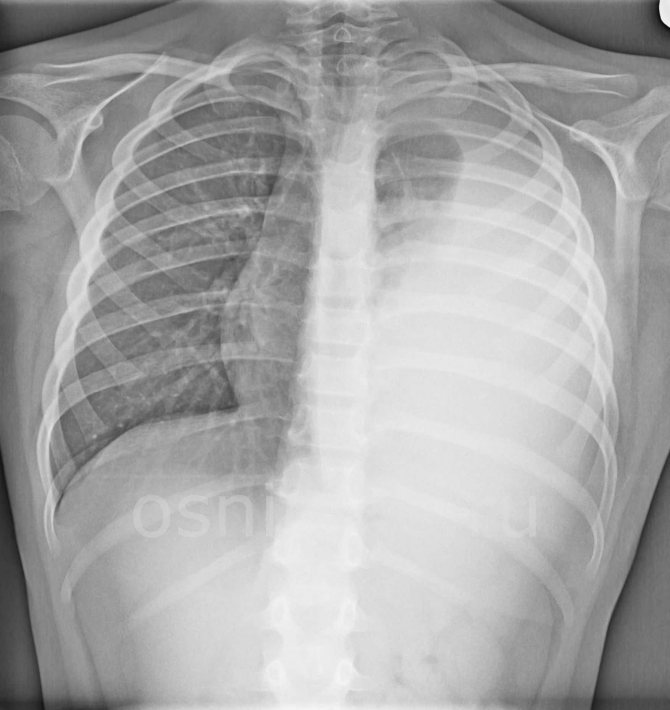
Изменения рентгеновской эмфиземы встречаются чаще и поражают левое и правое легкие. Однако иногда при локальной бронхоструктуре можно обнаружить компенсаторную эмфизему в виде повышенной пневматизации вокруг пневмосклероза и фиброза легочной ткани, области ателектазов и другие нефункциональные структуры. В этом случае вокруг локального затемнения на рентгенограмме появляются участки повышенной воздушности.
По рентгенограммам определяются следующие виды эмфиземы:
- Первичный — возникает в результате сужения просвета бронхов. Это ранняя форма, при которой изменения претерпевают регресс.
- Вторичная — хроническая эмфизема, при которой возникает закупорка бронхов патологическим содержимым.
- Третичный — местный пневмоторакс, при котором наблюдается усиление аэрации в некоторых частях легочных полей.
Если рентген показывает, что половина грудной клетки задохнулась, это называется пневмотораксом.
Эта патология часто осложняет течение буллезного пневмоторакса. Легкое прижимается к корню, за счет чего нарушается его структура. Органы средостения (сердце, магистральные сосуды, пищевод) перемещаются в здоровую часть грудной клетки.
Клинически у пациента проявляются симптомы острой дыхательной недостаточности и требуется хирургическое лечение: пункция плевральной полости.
Эмфизема средостения, или пневмомедиастинум, — это патологическое состояние, заключающееся в инфильтрации воздухом клетчатки средостения [4].
Считается, что спонтанная эмфизема средостения (СЭС) — редкое, самостоятельное заболевание, характеризующееся доброкачественным течением и возникающее без определенных причин, оно поражает в основном мужчин молодого возраста [9, 19, 23, 36].
Первое упоминание о СЭС датировано 1617 г., когда акушерка королевы Франции Louise Bourgeois в своих воспоминаниях описала внезапно возникшую у нее при родах одутловатость шеи [12]. Данное патологическое состояние впервые описал Rene Laennec в 1819 г. в трактате «О выслушивании стетоскопом» [24]. О СЭС как о самостоятельном заболевании первым сообщил Louis Hamman [5, 10, 19, 23, 25] в 1939 г. Он описал грубую крепитацию, синхронную с сердечными сокращениями, которая аускультативно выслушивается вдоль левого края грудины в третьем-шестом межреберьях, не исключая и другие зоны, в положении сидя. Этот клинический симптом получил название симптома Хэммана.
Патофизиологию данного заболевания на основании экспериментов на лабораторных животных описали в 1944 г. M. Macklin и С. Macklin [5, 10, 23, 25]. В эксперименте на животных они показали, что СЭС возникает в результате резкого понижения градиента давления между альвеолами и межуточной тканью легких, что приводит к разрыву альвеол. Описанный механизм в сочетании с патологическими изменениями альвеоляро-капиллярной мембраны и/или интерстициальной ткани легких может привести к прорыву альвеолы в межуточное пространство [31]. Прорыв альвеолы в легочный интерстиций ведет к накоплению в нем воздуха, который распространяется вдоль градиента давления, периваскулярно и перибронхиально, центростремительно к воротам легких, а затем в средостение (эффект Macklin) [20]. Это происходит потому, что давление в средостении ниже, чем на периферии легких. Большинство авторов сходятся во мнении, что заболевание возникает в результате разрыва терминальных альвеол, расположенных в корне сегмента (доли) легкого и прилежащих к рыхлой клетчатке, окружающей сосуды и бронхи [5, 16, 23]. Оказавшись в средостении, воздух может распространяться на клетчаточные пространства шеи, мягких тканей грудной клетки, в полость сердечной сорочки и даже (в зависимости от количества) в забрюшинное клетчаточное пространство [8].
Частота СЭС у госпитализированных больных варьирует, по различным данным, от 1:3578 [16] до 1:44 511[25].
Существуют разные триггерные механизмы или факторы, способствующие возникновению СЭС. I. Macia и соавт. [25] считают целесообразным разделять эти факторы на: предрасполагающие — вредные привычки и/или заболевания в анамнезе, которые создают благоприятные для развития заболевания условия, и провоцирующие — состояния, которые непосредственно предшествуют возникновению СЭС.
К предрасполагающим факторам многие авторы относят такие легочные заболевания, как бронхиальная астма [5, 9, 16, 19, 25, 29], воспалительные заболевания верхних дыхательных путей [5, 19], идиопатические фиброзирующие заболевания легких [9], хронические обструктивные заболевания легких [9]. Из перечисленных выше заболеваний, согласно публикациям в мировой литературе, только бронхиальная астма рассматривается как предрасполагающий фактор в развитии СЭС практически всеми авторами [5, 9, 16, 19, 25, 29, 35, 36]. J. Chapdelaine и соавт. [11] установили это заболевание в анамнезе почти у 50% больных, A. Newcomb и C. Clarke [29] — у 39% пациентов с СЭС. Нужно отметить, что в мировой литературе авторы редко связывают развитие СЭС с буллезной эмфиземой легких. А.Г. Высоцкий [2] описал 4 наблюдения пневмомедиастинума как осложнения локальной буллезной эмфиземы легких. И.И. Платов и В.С. Моисеев [4] считают, что развитие СЭС связано с теми же причинами, которые приводят к развитию спонтанного пневмоторакса, а именно с буллезной болезнью, кистозными образованиями легких врожденного генеза, респираторными воспалительными заболеваниями.
Некоторые авторы полагают, что курение является предрасполагающим фактором в развитии заболевания [9, 25]. J. Macia и соавт. [25] сравнили количество курильщиков, больных СЭС, с количеством курильщиков среди населения Каталонии (Испания), что составило 34,1 и 37,5%, соответственно. I. Abolnik и соавт. [6] отметили, что количество курильщиков среди больных СЭС незначительно отличалось от таковых в общей популяции.
Описано много провоцирующих факторов, которые непосредственно могут вызвать развитие заболевания. Следует выделить пробу Вальсальвы, интенсивный кашель, чихание, сильную рвоту, истерический крик, роды, акт дефекации, физическую нагрузку, бронхоспазм, спирометрию, игру на духовых инструментах, надувание шаров, употребление ингаляционных наркотических веществ [1, 5, 9, 10, 18, 23, 25, 26, 28, 32].
В сообщении М. Caceres и соавт. [9] доминирующим среди провоцирующих факторов была рвота, которая предшествовала началу заболевания в 36% наблюдений, на втором месте по частоте был приступ бронхиальной астмы, это состояние отмечалось у 21% больных. Кашель также является одним из частых триггерных факторов, и по разным данным, предшествует СЭС в 7,3% [25] и в 40% наблюдений [28]. Описано также возникновение СЭС на фоне диабетического кетоацидоза [36], химиотерапии [34], болезни Ходжкина [21].
Однако не всегда удается выявить предрасполагающие и/или провоцирующие факторы, СЭС нередко возникает в покое [9].
О разнообразии симптомов клинической манифестации СЭС сообщалось многими авторами [25, 36]. Чаще всего отмечается триада клинических симптомов — загрудинная боль (являющаяся самым частым и постоянным симптомом), затруднение дыхания, одутловатость шеи [1, 5, 15, 16, 19, 25, 29, 35, 36]. I. Abolnik и соавт. [6] отмечали наличие боли за грудиной у 88% больных СЭС, I. Macia и соавт. [25] — у 85%, M. Gerazounis и соавт. [16] — у 72,7%, G. Koullias и соавт. [23] — у 66,6%, M. Caceres и соавт. [9] — у 54% больных. Пациент также может предъявлять жалобы на боль в горле, спине, плече, пояснице, слабость, дисфагию, одинофагию, ринофонию, изменение тембра голоса. Некоторые авторы к симптомам заболевания относят и кашель, хотя он еще является и провоцирующим возникновение СЭС фактором [23]. М. Caceres и соавт. и G. Koullias и соавт. выделяли кашель как один из симптомов заболевания, он отмечался в 41 и 32% собственных наблюдений СЭС и являлся соответственно вторым и третьим по частоте симптомом после загрудинной боли [9, 23].
Из клинических симптомов заболевания, выявляемых при физикальном обследовании, чаще всего отмечается подкожная эмфизема мягких тканей шеи и/или груди [1, 2, 5, 7, 16, 25, 36]. В зависимости от количества воздуха, поступившего в клетчатку средостения, эмфизема мягких тканей может распространяться на область лица и нижних отделов грудной клетки, но это бывает редко [5]. В сообщении I. Macia и соавт. [25] у 95% пациентов с СЭС при пальпации определялась подкожная эмфизема мягких тканей, у 66% — шеи и у 29% больных — грудной стенки. J. Jougon и соавт. [19] констатировали наличие этого симптома у 100% больных СЭС. M. Gerazounis и соавт. [16] описали наличие ринофонии (гнусавости) у 5 пациентов, которая отмечалась совместно с эмфиземой мягких тканей шеи и развивалась вследствие диссекции воздухом тканей ретрофарингеального клетчаточного пространства. Этот симптом довольно редкий, но встречаются наблюдения, в которых он служит первым проявлением СЭС и основным клиническим симптомом заболевания [17].
Симптом Хэммана нельзя назвать специфичным для СЭС, так как, по утверждению Ю.В. Халева [5], подобная крепитация может выслушиваться и при левостороннем пневмотораксе без медиастинальной эмфиземы, а также при буллезной эмфиземе язычковых сегментов, пневмоперитонеуме с высоким стоянием диафрагмы, расширении желудка. Распространенность симптома Хэммана у больных СЭС, по данным разных источников, варьирует от 0 до 56% [6, 9, 10, 15, 23, 25, 29, 36].
При пневмомедиастинуме у больных также могут иметь место уменьшение сердечной тупости, глухость сердечных тонов при аускультации. I. Abolnik и соавт. [6] у 2 больных СЭС отмечали наличие парадоксального пульса. У большинства больных может быть один или несколько симптомов, но иногда при объективном исследовании не удается выявить ни одного симптома [5].
Основными методами диагностики СЭС являются рентгенография груди в прямой и боковых проекциях, КТ груди и рентгеноконтрастное исследование пищевода.
A. Yellin и соавт. [36] указали на необходимость выполнения рентгенографии (как рутинного метода первичной диагностики) всем пациентам молодого возраста с болью в груди неясного генеза и затруднением дыхания. По данным многих авторов, этот метод исследования оказался информативным у абсолютного большинства больных СЭС [6, 16, 23, 36], при этом они подчеркивают необходимость выполнения исследования в двух проекциях — прямой и боковой, потому что при небольшом скоплении газа в средостении при обзорной рентгенографии груди в прямой проекции пневмомедиастинум может быть не выявлен [23, 25].
При возникновении пневмомедиастинума на рентгеновском снимке обнаруживаются полосы просветления или пузырьки газа, окружающие органы средостения, приподнимающие медиастинальную плевру и часто распространяющиеся на шею и/или грудную стенку [14].
S. Bejvan и J. Godwin [8] сообщают, что при рентгенографии в прямой проекции свободный газ в средостении часто выявляется по левому контуру сердца и покрывает внутреннюю поверхность медиастинальной плевры, создавая хорошо заметную плевральную линию латеральнее легочного ствола и дуги аорты. На рентгенограммах в боковой проекции свободный газ образует линии просветления вдоль контуров восходящей аорты, дуги аорты и ее ветвей, легочных артерий и трахеи с главными бронхами [8]. Газ также локализуется вдоль линии прикрепления диафрагмы к грудине, вдоль вилочковой железы и плечеголовных вен [13].
Полипозиционная рентгенография — основной и очень эффективный метод исследования при данном заболевании, но если имеется инфильтрация газом мягких тканей грудной стенки, то его информативность сводится практически к нулю. В таких ситуациях, а также в случае настороженности по отношению к заболеваниям с похожей клинической картиной и при необходимости установления причины заболевания, если рентгенологический метод недостаточен, целесообразно выполнение КТ груди [30]. T. Kaneki и соавт. [20] отметили, что у 30% пациентов с СЭС при рентгенографии не удалось выявить пневмомедиастинум, окончательный диагноз был установлен при КТ груди. G. Koullias и соавт. [23] выполняли КТ после первичного рентгенологического исследования всем 25 больным, хотя и считали рентгенографию «золотым стандартом» диагностики СЭС, так как оба этих диагностических метода в 100% наблюдений оказались информативными в отношении пневмомедиастинума. КТ, несомненно, наиболее эффективный метод диагностики пневмомедиастинума [20], так как с его помощью легко выявляется наличие газа в средостении и при поперечных сечениях хорошо определяется его анатомическая локализация. Однако следует отметить, что по простоте выполнения и лучевой нагрузке на пациента этот метод проигрывает рентгенографии, также не стоит забывать об экономическом аспекте. A. Newcomb и C. Clarke [29] считают, что если пневмомедиастинум определяется с помощью рентгенографии и нет подозрения на присутствие какого-либо грозного заболевания как причины этого патологического состояния, то можно ограничиться только этим методом диагностики.
В некоторых наблюдениях СЭС, приведенных в мировой литературе, выполнялось рентгеноконтрастное исследование пищевода. Этот дополнительный метод диагностики применялся в тех ситуациях, когда необходимо было исключить наличие такого опасного состояния, как разрыв пищевода. Используется водорастворимый контрастный препарат и/или взвесь бария сульфата [15, 16, 19, 36]. D. Weissberg [35] пользовался этим методом исследования с целью исключения разрыва пищевода, если возникновению СЭС предшествовала рвота.
В число дополнительных методов исследования при данном заболевании входят эзофагоскопия, бронхоскопия и электрокардиография. Эти методы являются вспомогательными и применяются для подтверждения диагноза СЭС в сомнительных ситуациях.
Дифференциальная диагностика СЭС проводится с заболеваниями сердечно-сосудистой (острый коронарный синдром, перикардит), дыхательной (спонтанный пневмоторакс, эмболия легочной артерии, перфорация трахеобронхеального дерева) и пищеварительной (спонтанный разрыв пищевода) систем [32].
По мнению зарубежных авторов [15, 25, 29, 35, 36] оптимальные сроки стационарного наблюдения и лечения больных СЭС составляют от 2 до 5 дней.
СЭС хорошо поддается консервативному лечению, которое включает постельный режим, обезболивание и оксигенотерапию [6, 9, 15, 23, 29]. При этом наблюдается довольно быстрая регрессия симптомов и в большинстве наблюдений происходит полное разрешение пневмомедиастинума к 8-м суткам [29, 36]. Обычно вскоре после прорыва альвеол в легочный интерстиций они спадаются, так как давление в них снижается и прекращается поступление воздуха [19]. G. Koullias и соавт. [23] всем пациентам проводили антибактериальную профилактику медиастинита. Они использовали третье поколение цефалоспоринов с добавлением к терапии клиндамицина при подозрениях на перфорацию пищевода и когда заболевание сопровождалось повышением температуры тела и лейкоцитозом. Очень редко эмфизема клетчатки шеи, грудной и брюшной стенок, лица прогрессирует и развивается напряженный пневмомедиастинум. Средостение при этом, по выражению Зауербруха, «раздувается как шар», тонкостенные магистральные вены средостения сдавливаются с падением сердечной деятельности, нарушением дыхания и возможным смертельным исходом [3]. В таких ситуациях показана верхняя медиастинотомия по Tiegel с туннелизацией претрахеальной клетчатки до уровня бифуркации трахеи с дренированием средостения и последующей аспирацией, что обеспечивает декомпрессию средостения [4]. J. Moore и соавт. [27] у детей грудного возраста с напряженной эмфиземой средостения выполняли дренирование средостения через субксифоидный доступ. Для декомпрессии мягких тканей и средостения при данном осложнении некоторые авторы предлагают супрастернальную пункцию средостения и стернотомию [33], пункцию надключичных областей [6] и трахеостомию [22]. Если, несмотря на эти меры, наблюдается нарастание напряженной эмфиземы средостения, требуется срочная чресплевральная широкая медиастинотомия [4].
Описаны единичные наблюдения рецидива СЭС [16, 25]. Первыми в литературе рецидив заболевания описали A. Yellin и соавт. [36], они наблюдали пациентов в течение 52 мес после выписки из стационара, повторное возникновение эмфиземы средостения у одного пациента произошло через 14 мес после первого эпизода без предрасполагающих причин.
Таким образом, спонтанная эмфизема средостения является заболеванием, поражающим чаще молодых мужчин трудоспособного возраста. Ее возникновение требует дифференциальной диагностики с рядом серьезных патологических состояний. В редких ситуациях напряженная эмфизема средостения может привести к гемодинамическим и дыхательным нарушениям.